Accents thérapeutiques dans la maladie au stade avancé
Auteure:
Prof. Dre méd. Isabell Witzel
Klinik für Gynäkologie, Universitätsspital Zürich
E-mail: isabell.witzel@usz.ch
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Dans le traitement du cancer du sein métastatique HER2 positif, des schémas d’association innovants ont montré leur efficacité, comme le démontrent les analyses présentées au congrès ASCO 2024. Des données pertinentes ont également été obtenues dans la maladie triple négative, associée à un pronostic défavorable.
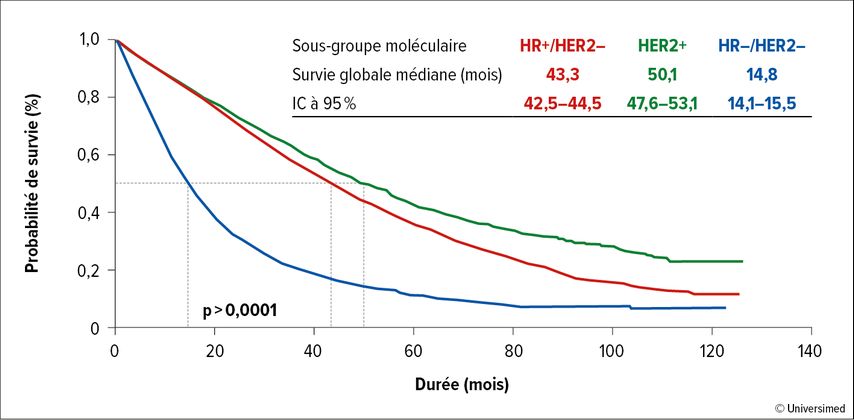
Une analyse française réalisée dans le contexte du cancer du sein métastatique a montré que le pronostic est le plus favorable chez les patient·es dont la maladie est HER2 positive, tandis que le cancer triple négatif est associé aux résultats les moins bons (Fig. 1).1 La diversité des traitements disponibles dans la maladie HER2 positive a permis d’obtenir un tel bienfait en termes de survie globale.
Fig. 1: Probabilité de survie dans le cancer du sein métastatique en fonction du sous-type moléculaire (modifiée d’après Deluche E et al.)1
On dispose de deux anticorps monoclonaux spécifiques d’HER2, le trastuzumab et le pertuzumab, et de trois inhibiteurs de tyrosine kinase, le lapatinib, le tucatinib et le nératinib. Le T-DM1 et le trastuzumab déruxtécan appartiennent au groupe des conjugués anticorps-médicament ciblant HER2. Dans leurs lignes directrices, l’Arbeitsgemeinschaft Gynäkologische Onkologie (Groupe de travail en gynéco-oncologie) et la Deutsche Krebsgesellschaft (Société allemande du cancer) désignent l’association d’un taxane (docétaxel, paclitaxel ou nab-paclitaxel) et de la double inhibition d’HER2 par trastuzumab et pertuzumab comme stratégie standard de première ligne dans le cancer du sein métastatique HER2 positif.2
Non-infériorité de l’éribuline
L’étude japonaise de phaseIII EMERALD (JBCRG-M06) a comparé l’utilisation de l’éribuline et celle d’un taxane (docétaxel ou paclitaxel), chacun associé au trastuzumab/pertuzumab, dans le traitement de première ligne du cancer du sein HER2 positif localement avancé ou métastatique. L’objectif de l’étude était de démontrer la non-infériorité du schéma à base d’éribuline. Un traitement (néo)adjuvant devait avoir été terminé au moins six mois avant le recrutement.
La survie sans progression (PFS), définie comme le critère d’évaluation primaire, ne différait pas entre les deux schémas.3 La survie sans progression (PFS) médiane était de 14,0 mois dans le bras expérimental et de 12,9 mois dans le bras témoin (HR: 0,95; p=0,6817). Aucun des sous-groupes évalués n’a bénéficié de l’éribuline dans une mesure particulière. Il n’y a pas non plus eu de différence en termes de survie globale (HR: 1,09), ni en termes de taux de réponse global (76,8% vs 75,2%). Les deux bras de l’étude ont atteint des taux de bénéfice clinique de près de 90%.
Le profil d’effets secondaires de l’association à base d’éribuline était dominé par la neutropénie et la neuropathie sensorielle, celui de l’association à base de taxane, par les manifestations cutanées, la diarrhée et la neuropathie sensorielle. Les auteur·es ont conclu que l’éribuline en association au trastuzumab/pertuzumab constituait une alternative au traitement par taxane en première ligne.
Endocrinothérapie plus traitement ciblant HER2
Si aucune chimiothérapie n’est possible ou souhaitée dans le cancer métastatique HER2 positif, la stratégie consistant à associer un traitement ciblant HER2 et une endocrinothérapie (ET) est envisageable en présence de maladie positive pour les récepteurs hormonaux (HR).2
L’étude PERTAIN avait déjà démontré qu’il était possible d’obtenir une longue PFS même sans chimiothérapie; sous trastuzumab/pertuzumab plus inhibition de l’aromatase, la PFS médiane était de près de 22 mois.4 De même, l’étude monarcHER a prouvé l’efficacité de l’association de l’inhibiteur CDK4/6 abémaciclib plus fulvestrant avec le trastuzumab après au moins deux traitements antérieurs dans le cadre d’un traitement de la maladie métastatique (PFS médiane: 8,3 mois).5
L’étude PATRICIA évaluait l’association d’un inhibiteur de CDK4/6, le palbociclib, avec le trastuzumab et une ET; la comparaison a été effectuée avec un traitement au choix du médecin.6 Les patient·es présentaient un cancer du sein avancé HR positif/HER2 positif de sous-type luminal A ou B selon la signature génique PAM50. Dans la maladie au stade avancé, au moins une ligne de traitement avait déjà été administrée. L’examen des caractéristiques initiales montre qu’il existe un déséquilibre dans la proportion de patient·es présentant une maladie métastatique au moment du diagnostic initial (42,1% dans le bras expérimental vs 28,6% dans le bras de contrôle), qui pourraient mieux répondre au traitement.
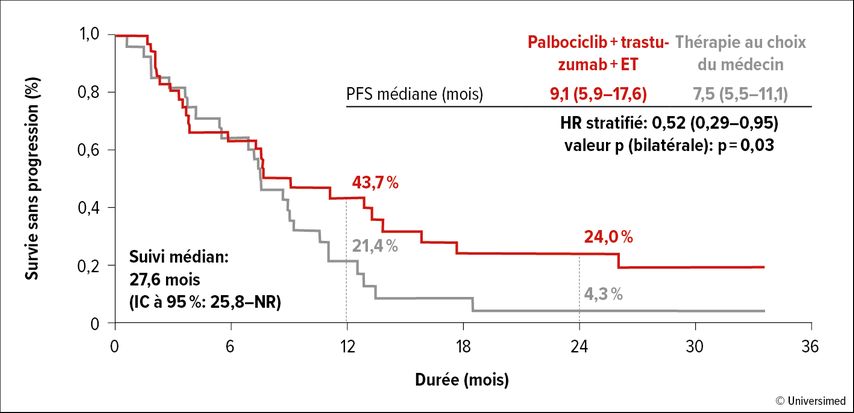
Le critère d’évaluation primaire était la PFS selon les investigateurs. À cet égard, un bienfait significatif a pu être obtenu avec le schéma à base de palbociclib (PFS médiane: 9,1 vs 7,5 mois; HR: 0,52; p=0,03; Fig. 2). Les traitements utilisés présentaient un profil d’effets secondaires similaire. Selon l’algorithme en vigueur actuellement, le palbociclib en association avec le trastuzumab et un inhibiteur de l’aromatase est envisageable à partir de la deuxième ligne.2
Fig. 2: Étude PATRICIA: survie sans progression sous palbociclib plus trastuzumab et ET vs traitement au choix des médecins (modifiée d’après Ciruelos E et al.)6
Olaparib en cas de mutations BRCA ou PALB2
Dans le cas du cancer du sein métastatique triple négatif, le choix du traitement est établi en fonction d’une part du statut PD-L1 et d’autre part du résultat du test de mutation BRCA1/2. En présence d’une mutation BRCA1 ou BRCA2, la prescription d’inhibiteurs de PARP est possible à différents moments.2 Les lignes directrices suggèrent l’utilisation de l’olaparib en cas de mutations somatiques BRCA1/2 et de mutations de la voie germinale PALB2. Il ne s’agit pas d’une recommandation forte. Cela pourrait maintenant changer au vu des données des cohortes de prolongation de l’étude de phaseII TBCRC 048.
L’olaparib en monothérapie a été évalué dans la phase de prolongation de l’étude chez des patient·es atteint·es d’un cancer du sein métastatique, quel que soit le sous-type, et présentant des mutations de la voie germinale PALB2 ou des mutations somatiques BRCA1/2.7 Les deux cohortes comprenaient 13% de patient·es dont le cancer était triple négatif. Avant le recrutement, au moins deux chimiothérapies avaient été administrées dans le cadre d’un traitement de la maladie métastatique.
Dans le groupe de mutation PALB2, 75% des patient·es ont répondu au traitement et la PFS médiane était de 9,6 mois. En présence de mutations BRCA1/2, une PFS médiane de 7,2 mois a été atteinte; la réponse s’est maintenue pendant 12,4 mois. Comme le suggèrent ces données, l’olaparib en monothérapie est une option pour les patient·es atteint·es d’un cancer du sein triple négatif et qui portent une mutation germinale PALB2 ou une mutation somatique BRCA1/2.
Littérature:
1 Deluche E et al.: Contemporary outcomes of metastatic breast cancer among 22,000 women from the multicentre ESME cohort 2008-2016. Eur J Cancer 2020; 129: 60-70 2 AGO e.V.: Diagnosis and treatment of patients with early and advanced breast cancer. En ligne sur https://www.ago-online.de 3 Yamashita T et al.: Trastuzumab and pertuzumab in combination with eribulin mesylate or a taxane as first-line chemotherapeutic treatment for HER2-positive, locally advanced or metastatic breast cancer: results of a multicenter, randomized, non-inferiority phase 3 trial in Japan (JBCRG-M06/EMERALD). J Clin Oncol 2024; 42(Suppl. 16): Abstr. #1007 4 Rimawi M et al.: First-line trastuzumab plus an aromatase inhibitor, with or without pertuzumab, in human epidermal growth factor receptor 2-positive and hormone receptor-positive metastatic or locally advanced breast cancer (PERTAIN): a randomized, open-label phase II trial. J Clin Oncol 2018; 36(28): 2826-35 5 Tolaney SM et al.: Abemaciclib plus trastuzumab with or without fulvestrant versus trastuzumab plus standard-of-care chemotherapy in women with hormone receptor-positive, HER2-positive advanced breast cancer (monarcHER): a randomised, open-label, phase 2 trial. Lancet Oncol 2020; 21(6): 763-75 6 Ciruelos E et al.: Primary results from PATRICIA Cohort C (SOLTI-1303), a randomized phase II study evaluating palbociclib with trastuzumab and endocrine therapy in pretreated HER2-positive and PAM50 luminal advanced breast cancer. Clin Oncol 2024; 42(Suppl. 16): Abstr. #1008 7 Tung NM et al.: TBCRC 048 (olaparib expanded) expansion cohorts: phase II study of olaparib monotherapy in metastatic breast cancer patients with germline mutations in PALB2 or somatic mutations in BRCA1 or BRCA2. J Clin Oncol 2024; 42(Suppl. 16): Abstr. #1021
Das könnte Sie auch interessieren:
Cancer de l’endomètre métastatique, avancé et récidivant
L’association d’inhibiteurs de point de contrôle et de chimiothérapie peut être considérée comme une nouvelle norme thérapeutique dans les cancers de l’endomètre avec déficit de ...
Parfois, il suffit d’attendre
Compte tenu de la multitude d’options thérapeutiques ciblées et immunothérapeutiques désormais disponibles, la prise en charge du carcinome à cellules rénales en situation adjuvante et ...
Les néoplasies myélodysplasiques: stratégies thérapeutiques personnalisées
Les progrès réalisés dans la compréhension moléculaire des néoplasies myélodysplasiques (MDS, myelodysplastic syndrome) ont permis de mettre au point des approches thérapeutiques ...