Chemotherapiefreie Optionen für diverse Subgruppen
Autor:
Prof. Dr. med. Jens Huober
Brustzentrum, Kantonsspital St. Gallen
E-Mail: jens.huober@kssg.ch
Im Management des HR-positiven/HER2-negativen fortgeschrittenen Mammakarzinoms steht mittlerweile eine vielfältige Therapielandschaft zur Verfügung. Mit zielgerichteten Ansätzen zusätzlich zur endokrinen Therapie lässt sich ein breites Spektrum an Patient:innen abdecken.
Die Studien PALOMA-2, MONALEESA-2 und MONARCH 3 haben im Erstlinien-Setting des fortgeschrittenen Hormonrezeptor(HR)-positiven/HER2-negativen Mammakarzinoms signifikante Verlängerungen des progressionsfreien Überlebens (PFS) durch die Zugabe der CDK4/6-Inhibitoren Palbociclib, Ribociclib bzw. Abemaciclib zur endokrinen Therapie (ET) gezeigt.1–3 Im Fall einer neuerlichen Progression besteht eine Option darin, bei gleichzeitiger Fortführung der CDK4/6-Inhibition die endokrine Therapie umzustellen. Dies wurde in der postMONARCH-Studie und der MAINTAIN-Studie erfolgreich umgesetzt.4,5 Eine endgültige Beurteilung dieser Strategie steht allerdings noch aus.
Akteure am PI3K/AKT/mTOR-Pathway
Eine zentrale Rolle beim HR-positiven Mammakarzinom spielt der PI3K/AKT/mTOR-Pathway, an dem verschiedene Therapeutika ansetzen. Als Landmark-Studie für die PI3K-Inhibition gilt die SOLAR-Studie, in der Patient:innen mit einer Progression während oder nach der Aromatase-Inhibitor(AI)-Therapie entweder Fulvestrant plus Alpelisib oder Fulvestrant plus Placebo erhielten.6
Die Gruppe mit PI3K-Mutation profitierte in signifikantem und klinisch relevantem Ausmass von der Kombination (medianes PFS: 11,0 vs. 5,7 Monate; HR: 0,65). In einer sehr kleinen Gruppe von Patient:innen mit vorheriger CDK4/6-Inhibitortherapie (n=20) ergab sich auch ein Vorteil durch die Kombinationstherapie mit Alpelisib (5,5 vs. 1,8 Monate; HR: 0,48).
Von Vorteil erwies sich auch die Zugabe des AKT-Inhibitors Capivasertib zu Fulvestrant in der CAPItello-Studie.7 Die Patient:innen waren unter einer Behandlung mit Aromatasehemmern (AI) im adjuvanten oder metastasierten Setting progredient geworden. Im Vergleich zu Placebo plus Fulvestrant resultierte eine signifikante und klinisch relevante PFS-Verlängerung sowohl in der Gesamtpopulation (7,2 vs. 3,6 Monate; HR: 0,60) als auch in der Gruppe mit AKT-Pathway-Alterationen (7,3 vs. 3,1 Monate; HR: 0,50). Auch die CDK4/6-Inhibitor-vorbehandelten Patient:innen (70%) profitierten von Capivasertib plus Fulvestrant.
Palbociclib plus Inavolisib
Die INAVO120-Studie evaluierte die Kombination aus dem CDK4/6-Inhibitor Palbociclib und dem PI3Kα-Inhibitor Inavolisib bei Patient:innen mit PIK3CA-mutiertem HR-positivem Mammakarzinom und Progression während bzw. nach einer adjuvanten ET. Als Vergleichsregime gelangte Placebo plus Palbociclib zum Einsatz. In beiden Armen wurde zusätzlich Fulvestrant verabreicht. Die Zugabe von Inavolisib ergab eine signifikante Zunahme des medianen PFS von 7,3 auf 15,0 Monate (HR: 0,43).8Auch konnte eine Verzögerung der Zeit bis zur Chemotherapie im Prüfarm nachgewiesen werden (nicht erreicht vs. 15,0 Monate; HR: 0,54).9
Landmark-Daten zum selektiven Östrogenrezeptor-Degrader Elacestrant stammen aus der EMERALD-Studie. In dieser Studie wurden Patient:innen mit HR-positivem metastasiertem Brustkrebs nach endokrinen Vortherapien und obligat einer CDK4/6-Inhibitortherapie zu Elacestrant oder einer endokrinen Therapie nach Wahl (zumeist Fulvestrant, 70%) randomisiert. Elacestrant erwies sich besonders in der ESR1-mutierten Population als effektiv (medianes PFS: 3,78 vs. 1,87 Monate; HR: 0,504).10 Noch deutlicher fiel der PFS-Unterschied in der Subgruppe aus, die vorab zumindest ein Jahr lang einen CDK4/6-Inhibitor erhalten hatte (8,61 vs. 1,91 Monate; HR: 0,410).11
ADC: T-DXd und SG
Von hohem Interesse sind Antikörper-Chemotherapie-Konjugate (ADCs) wie Trastuzumab Deruxtecan (T-DXd), das in der DESTINY-Breast04-Studie beim HER2-low-Mammakarzinom (d.h. HER2 1+ oder 2+/FISH–) untersucht wurde.12 In der HR-positiven Kohorte (90% der Patient:innen) führte T-DXd vs. TPC (Chemotherpie nach Wahl des Prüfarztes) zu signifikanten Verlängerungen von PFS (9,6 vs. 4,2 Monate; HR: 0,37) und Gesamtüberleben (OS; 23,9 vs. 17,6 Monate; HR: 0,69).
Die DESTINY-Breast06-Studie schloss zusätzlich Patient:innen mit HER2-ultralow-Tumoren ein (d.h. Anfärbung bei <10% der Zellen). Weiterhin hatten alle Patient:innen einen HR-positiven Tumor und waren weniger stark vorbehandelt (keine Chemotherapie in der Metastasierung).13 Unter T-DXd konnten im Vergleich zu TPC PFS-Verlängerungen sowohl bei HER2-low-Karzinomen (13,2 vs. 8,1 Monate; HR: 0,62) als auch bei HER2-ultralow-Erkrankung (13,2 vs. 8,3 Monate; HR: 0,78) erzielt werden.
Das gegen Trop2 gerichtete ADC Sacituzumab Govitecan verlängerte in der TROPiCS-02-Studie verglichen mit TPC bei massiv vorbehandelten Patient:innen das mediane PFS (5,5 vs. 4,0 Monate; HR: 0,65) sowie das OS (14,5 vs. 11,2 Monate; HR: 0,79).14 Ebenso verbesserte das Trop2-gezielte ADC Datopotamab Deruxtecan in der TROPION-Breast01-Studie in der HR+/HER2– Situationnach unterschiedlichen Vortherapien inklusive CDK4/6-Inhibitionsignifikant das PFS im Vergleich zu einer Chemotherapie nach Wahl des Prüfarztes (6,9 vs. 4,5 Monate; HR: 0,64).15
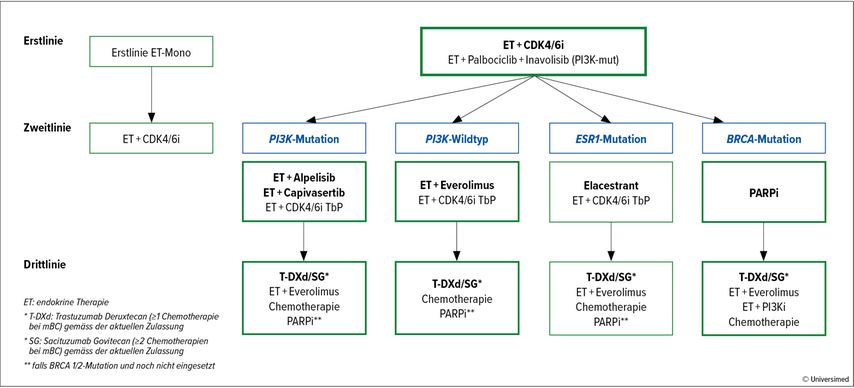
Ein aktueller Algorithmus für die Behandlung des HR+/HER2– Mammakarzinoms mit einem Rezidiv während oder nach der adjuvanten ET sieht beim Grossteil der Patient:innen eine Erstlinientherapie mit ET und CDK4/6-Inhibition vor (Abb. 1). Im Anschluss kommt ein individualisiertes Vorgehen je nach genetischem Set-up infrage, und T-DXd sowie SG stehen in den weiteren Linien zur Verfügung. Als weiteres Target sollte auch immer an eine BRCA 1- oder -2-Mutation gedacht werden, da hier mit den PARP-Inhibitoren zielgerichtete Therapien zur Verfüguntg stehen.
Abb. 1: Therapiealgorithmus beim Östrogenrezeptor-positiven/HER2-negativen Mammakarzinom mit Rezidiv nach oder unter der adjuvanten endokrinen Therapie (bevorzugte Therapien sind fett hervorgehoben, die übrigen sind weitere mögliche Optionen)
Literatur:
1 Finn RS et al.: Palbociclib and letrozole in advanced breast cancer. N Engl J Med 2016; 375(20): 1925-36 2 Hortobagyi GN et al.: Ribociclib as first-line therapy for HR-positive, advanced breast cancer. N Engl J Med 2016; 375(18): 1738-48 3 Goetz MP et al.: MONARCH 3: abemaciclib as initial therapy for advanced breast cancer. J Clin Oncol 2017; 35(32): 3638-46 4 Kalinsky K et al.: Abemaciclib plus fulvestrant vs fulvestrant alone for HR+, HER2- advanced breast cancer following progression on a prior CDK4/6 inhibitor plus endocrine therapy: primary outcome of the phase 3 postMONARCH trial. J Clin Oncol 2024; 42(Suppl. 17): Abstr. #LBA1001 5 Kalinsky K et al.: Randomized phase II trial of endocrine therapy with or without ribociclib after progression on cyclin-dependent kinase 4/6 inhibition in hormone receptor-positive, human epidermal growth factor receptor 2-negative metastatic breast cancer: MAINTAIN trial. J Clin Oncol 2023; 41(24): 4004-13 6 André F et al.: Alpelisib for PIK3CA-mutated, hormone receptor-positive advanced breast cancer. NEngl J Med 2019; 380(20): 1929-40 7 Turner N et al.: Capivasertib and fulvestrant for patients with aromatase inhibitor-resistant hormone receptor-positive/human epidermal growth factor receptor 2-negative advanced breast cancer: results from the Phase III CAPItello-291 trial. SABCS 2022; Abstr. #GS3-04 8 Jhaveri KL et al.: Inavolisib or placebo in combination with palbociclib and fulvestrant in patients with PIK3CA-mutated, hormone receptor-positive, HER2-negative locally advanced or metastatic breast cancer: phase III INAVO120 primary analysis. SABCS 2023; Poster #PD1-02 9 Juric D et al.: First-line inavolisib/placebo + palbociclib + fulvestrant in patients with PIK3CA-mutated, hormone receptor-positive, HER2 negative locally advanced/metastatic breast cancer who relapsed during/within 12 months of adjuvant endocrine therapy completion: INAVO120 phase III randomized trial additional analyses. J Clin Oncol 2024; 42(Suppl. 16): Abstr. #1003 10 Bidard F et al.: Elacestrant (oral selective estrogen receptor degrader) versus standard endocrine therapy for estrogen receptor-positive, human epidermal growth factor receptor 2-negative advanced breast cancer: results from the randomized phase III EMERALD trial. J Clin Oncol 2022; 40(28): 3246-56 11 Bardia A et al.: EMERALD phase 3 trial of elacestrant versus standard of care endocrine therapy in patients with ER+/HER2- metastatic breast cancer: updated results by duration of prior CDK4/6i in metastatic setting. SABCS 2022; Abstr. #GS3-01 12 Modi S et al.: Trastuzumab deruxtecan (T-DXd) versus treatment of physician’s choice in patients with HER2-low unresectable and/or metastatic breast cancer: updated survival results of the randomized, phase III DESTINY-Breast04 study. Ann Oncol 2023; 34(Suppl. 2): S334-90 13 Curigliano G et al.: Trastuzumab deruxtecan vs physician’s choice of chemotherapy in patients with hormone receptor-positive, human epidermal growth factor receptor 2-low or HER2-ultralow metastatic breast cancer with prior endocrine therapy: primary results from DESTINY-Breast06. J Clin Oncol 2024; 42(Suppl. 17): Abstr. #LBA1000 14 Tolaney SM et al.: Final overall survival (OS) analysis from the phase 3 TROPiCS-02 study of sacituzumab govitecan in patients with hormone receptor–positive/HER2-negative metastatic breast cancer. J Clin Oncol 2023; 41(Suppl. 16): Abstr. #1003 15 Bardia A et al.: Datopotamab deruxtecan vs chemotherapy in previously-treated inoperable or metastatic hormone receptor-positive, HER2-negative breast cancer: primary results from the randomised phase III TROPION-Breast01 trial. Ann Oncol 2023; 34(Suppl. 2): S1264-5
Das könnte Sie auch interessieren:
Erhaltungstherapie mit Atezolizumab nach adjuvanter Chemotherapie
Die zusätzliche adjuvante Gabe von Atezolizumab nach kompletter Resektion und adjuvanter Chemotherapie führte in der IMpower010-Studie zu einem signifikant verlängerten krankheitsfreien ...
Highlights zu Lymphomen
Assoc.Prof. Dr. Thomas Melchardt, PhD zu diesjährigen Highlights des ASCO und EHA im Bereich der Lymphome, darunter die Ergebnisse der Studien SHINE und ECHELON-1
Aktualisierte Ergebnisse für Blinatumomab bei neu diagnostizierten Patienten
Die Ergebnisse der D-ALBA-Studie bestätigen die Chemotherapie-freie Induktions- und Konsolidierungsstrategie bei erwachsenen Patienten mit Ph+ ALL. Mit einer 3-jährigen ...