Épisodes de fibrillation atriale asymptomatiques chez les patients porteurs de dispositifs cardiaques implantés: Qui doit recevoir une anticoagulation?
Auteurs:
Dr méd. Andrea Papa
Pr Dr méd. Christian Sticherling
Universitäres Herzzentrum
Universitätsspital Basel
E-mail: christian.sticherling@usb.ch
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Chez les patients porteurs de stimulateurs cardiaques, de défibrillateurs implantables ou d’enregistreurs en boucle, de brefs épisodes d’arythmie atriale, appelés «device-detected atrial fibrillation» (DDAF), sont souvent détectés lors de l’interrogation de ces dispositifs. On ignore s’il faut amorcer une anticoagulation orale chez les patients sans fibrillation atriale connue. Deux grands essais contrôlés et randomisés donnent un aperçu des avantages et des inconvénients potentiels d’un traitement anticoagulant.
Keypoints
-
Les DDAF sont des épisodes d’activité électrique atriale rapide détectés par des appareils cardiaques électriques implantables ou par des moniteurs cardiaques implantables.
-
L’incidence des DDAF est d’environ 30% à 3 ans.
-
Le risque annuel d’événement thromboembolique est très faible dans cette population (environ 1%).
-
Environ 25% des patients présentant des DDAF développent une fibrillation atriale clinique au cours des trois années suivantes.
-
Sur la base des études NOAH-AFNET 6 et ARTESiA, aucune recommandation générale n’est donnée concernant l’anticoagulation orale. Elle devrait toutefois être envisagée chez les patients présentant un risque thromboembolique très élevé (CHA2DS2-VASc >4).
La fibrillation atriale (FA) est le trouble du rythme cardiaque le plus fréquent et est associée à une mortalité et à une morbidité accrues, notamment en ce qui concerne les accidents vasculaires cérébraux (AVC), les infarctus du myocarde, l’insuffisance cardiaque et le déclin cognitif.1 La prévalence estimée est d’environ 2 à 4% dans le monde et passe à 9% chez les adultes de plus de 80 ans. On estime que le risque de survenue d’une FA au cours de la vie est de 1 personne sur 3 d’origine européenne à l’âge de 55 ans.
On parle de FA clinique lorsqu’un enregistrement ECG conventionnel à 12 dérivations ou à une dérivation de ≥30s montre un rythme cardiaque irrégulier sans ondes P détectables.
Chez les personnes âgées en particulier, la FA est souvent asymptomatique et se manifeste pour la première fois par une thromboembolie cérébrale. Environ 20% des accidents vasculaires cérébraux ont pour origine une FA. Si l’on recherche une FA tôt après un événement ischémique à l’aide d’une surveillance continue du rythme, comme un enregistreur en boucle implantable (ILR), on la retrouve chez 30% supplémentaires des patients victimes d’un AVC cryptogénique. Sur la base de ces observations, une grande attention est actuellement accordée à l’identification précoce des personnes présentant un risque plus élevé de FA. Deux grandes études randomisées publiées récemment ont cherché à savoir si l’instauration d’une anticoagulation orale (ACO) précoce dans la population présentant des épisodes asymptomatiques de FA détectés dans la mémoire des stimulateurs cardiaques implantés, des défibrillateurs automatiques implantables (DAI) et des enregistreurs en boucle, permettait de réduire le taux d’événements thromboemboliques, voire la mortalité.
«Device-detected atrial fibrillation»: la dimension du problème
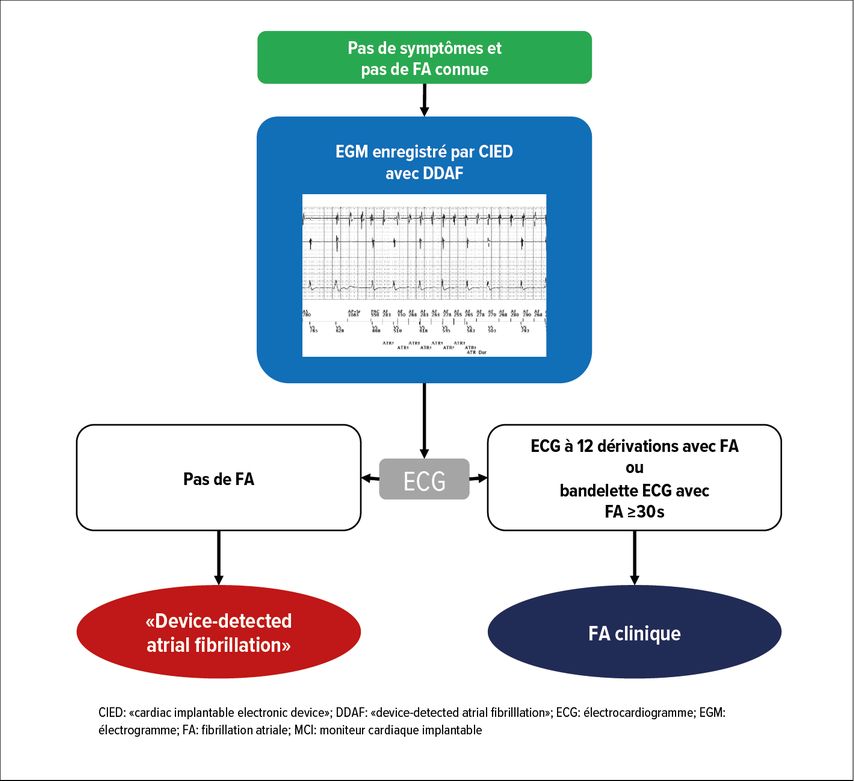
Les directives de l’ESC pour la prise en charge de la fibrillation atriale de 2024 ont établi le terme de «fibrillation atriale détectée via dispositif» («device-detected atrial fibrillation», DDAF), qui remplace les anciens termes «atrial high rate episodes» et «subclinical atrial fibrillation».1 La DDAF décrit une activité électrique atriale rapide, avec une fréquence atriale ≥175/min et une durée ≥5 minutes, détectée par des dispositifs électriques cardiaques implantables (CIED) ayant la possibilité d’enregistrer l’activité atriale, comme les stimulateurs cardiaques et les défibrillateurs, ou par des moniteurs cardiaques implantables. Comme les électrogrammes enregistrés peuvent contenir des artéfacts ou du bruit, une inspection visuelle minutieuse est nécessaire pour confirmer une arythmie atriale (Fig. 1). La DDAF est généralement découverte par hasard lors d’un contrôle de routine du CIED et est généralement asymptomatique.
Fig. 1: Diagnostic de la fibrillation atriale détectée par un appareil (DDAF). Les appareils électriques implantables cardiaques (CIED) avec une dérivation atriale peuvent surveiller le rythme auriculaire et enregistrer les données. Les moniteurs cardiaques implantables (MCI) surveillent en permanence l’activité électrique du cœur en enregistrant et en analysant un ECG bipolaire de surface (adaptée de Hindricks G et al.: Eur Heart J 2021; 42: 373-498)
L’incidence des DDAF chez les patients porteurs de CIED est d’environ 30%. Les épisodes très courts (<20s par jour) ne sont pas pertinents sur le plan clinique. Cependant, des épisodes prolongés de DDAF sont associés à un risque accru de fibrillation atriale clinique, d’accident vasculaire cérébral ischémique et d’événements cardiovasculaires graves.2
Risque thromboembolique en cas de fibrillation atriale clinique et infraclinique
Dans les premières études évaluant l’efficacité des antagonistes de la vitamine K par rapport au placebo, le taux moyen d’AVC chez les patients atteints de FA clinique sans traitement était de 5% par an et atteignait jusqu’à 12% par an en prévention secondaire. Les antagonistes de la vitamine K réduisent de 64% le risque d’AVC chez les patients atteints de FA par rapport au placebo, avec une réduction absolue du risque pour tous les AVC de 2,7% par an en prévention primaire et de 8,4% par an en prévention secondaire.3
Une méta-analyse de quatre grandes études randomisées portant sur 42411 patients recevant un anticoagulant oral non vitamine K (AOD, anticoagulant oral direct) et 29272 patients recevant de la warfarine a montré une efficacité significativement supérieure des AOD, par rapport à la warfarine, dans la prévention des AVC et des embolies systémiques (ES) (HR: 0,81; p<0,001). Les AOD ont également réduit de manière significative la mortalité globale (HR: 0,90; p=0,0003) et le risque d’hémorragie intracrânienne (HR: 0,48; p<0,001), mais ont augmenté le risque d’hémorragie gastro-intestinale (HR: 1,25; p=0,04).4
Avant l’ère des AOD, un risque annuel d’AVC de 1,7% était considéré comme le seuil pour amorcer une ACO chez les patients atteints de fibrillation atriale.5 Au cours des dix dernières années, après les études sur la FA avec les AOD, les directives ont recommandé une anticoagulation chez les patients présentant un risque annuel d’AVC de 1,0%. Ce déplacement vers le bas est en accord avec la plus grande sécurité des AOD. Un score CHA2DS2-VA <1 définit un groupe dont le risque annuel d’AVC et/ou d’ES est <1% et pour lequel il est possible de renoncer à une ACO en raison du bénéfice absolu minimal. Les lignes directrices de l’ESC de 2024 sur le traitement de la fibrillation atriale recommandent les AOD chez les patients atteints de FA dont le risque thromboembolique annuel est estimé à >0,6–1% (ce qui correspond à un score CHA2DS2-VA >2). Si le score CHA2DS2-VA est de 1, une ACO peut être envisagée.1
«Device-detected atrial fibrillation»
En 2009, l’étude TRENDS a montré que, dans une cohorte de patients porteurs de stimulateurs cardiaques ou de défibrillateurs et ayant au moins un facteur de risque d’AVC (insuffisance cardiaque, hypertension artérielle, âge ≥65 ans, diabète ou ES antérieure), le risque annualisé d’événements thromboemboliques pendant un suivi moyen de 1,4 an était de 1,1% pour les patients sans FA, de 1,1% pour les patients avec un faible fardeau de la FA (<5,5 heures) et à 2,4% pour les patients présentant un fardeau de la FA élevé (≥5,5 heures).6
L’étude ASSERT a également suggéré que les patients atteints de FA infraclinique présentaient un risque 2,5 fois plus élevé d’AVC ischémique, avec un risque absolu de 1,7% par an.7 Une autre analyse de la cohorte ASSERT a révélé que le risque d’AVC était presque exclusivement dû aux DDAF qui duraient plus de 24 heures (risque absolu de 3,1% par an; HR: 3,24; p=0,003), alors que le risque n’était pas significativement différent chez les patients présentant des épisodes de haute fréquence atriale (AHRE) de plus courte durée que chez les patients sans AHRE.8
Faut-il administrer une anticoagulation à tous les patients présentant des DDAF?
La question qui se pose maintenant est de savoir si l’ACO réduit le taux de complications thromboemboliques chez les patients présentant des DDAF et si un dépistage des DDAF est même éventuellement justifié. La première d’une série d’études randomisées portant sur la fibrillation atriale détectée via un appareil et l’anticoagulation a été l’étude LOOP.9 Dans cette étude, des patients danois âgés présentant au moins un facteur de risque supplémentaire d’AVC (score CHA2DS2-VASc ≥2) et âgés en moyenne de 75 ans ont été assignés soit à une surveillance par ILR soit à des soins standard (1:3) avec des visites annuelles. Dans le groupe ILR, une ACO a été instaurée lorsque les épisodes de FA duraient 6 minutes ou plus.
L’étude a montré que les moniteurs cardiaques implantables augmentent la détection des DDAF, ce qui conduit à l’instauration plus fréquente d’un traitement anticoagulant. Toutefois, le nombre d’AVC ou d’ES n’a pas été réduit dans le groupe ILR par rapport au groupe de contrôle (4,5% vs 5,6%; p=0,11). Des hémorragies plus importants ont été observés chez 4,3% des patients du groupe ILR vs 3,5% dans le groupe de contrôle (p=0,11).
Il convient de noter que 91% des patients atteints de FA dans le groupe ILR et 86,5% dans le groupe de contrôle ont bénéficié d’une ACO. Malgré un taux de détection des DDAF/FA trois fois plus élevé (32% vs 12%) dans le groupe ILR, cela n’a pas entraîné une diminution du risque d’AVC. Deux études récemment publiées (GUARD-AF10, STROKESTOPP II11) confirment que si le dépistage dans de grandes populations permet de détecter davantage de DDAF/FA, le début de l’ACO qui en découle ne réduit malheureusement pas le risque d’AVC.
Les AOD en cas de DDAF – les études NOAH-AFNET 6 et ARTESiA
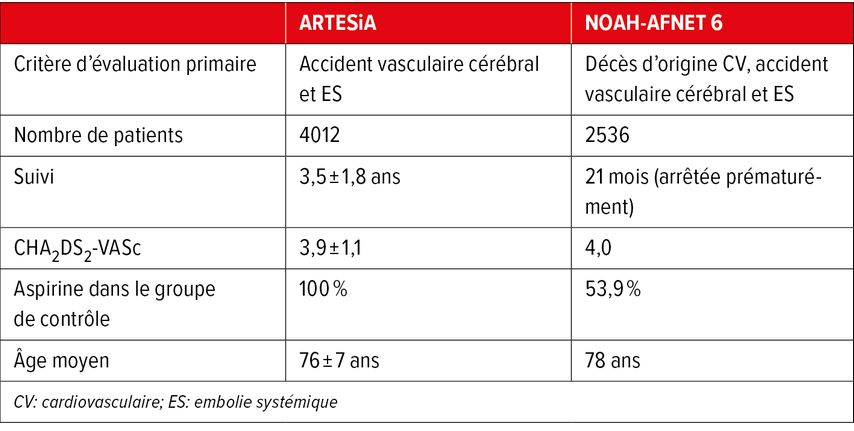
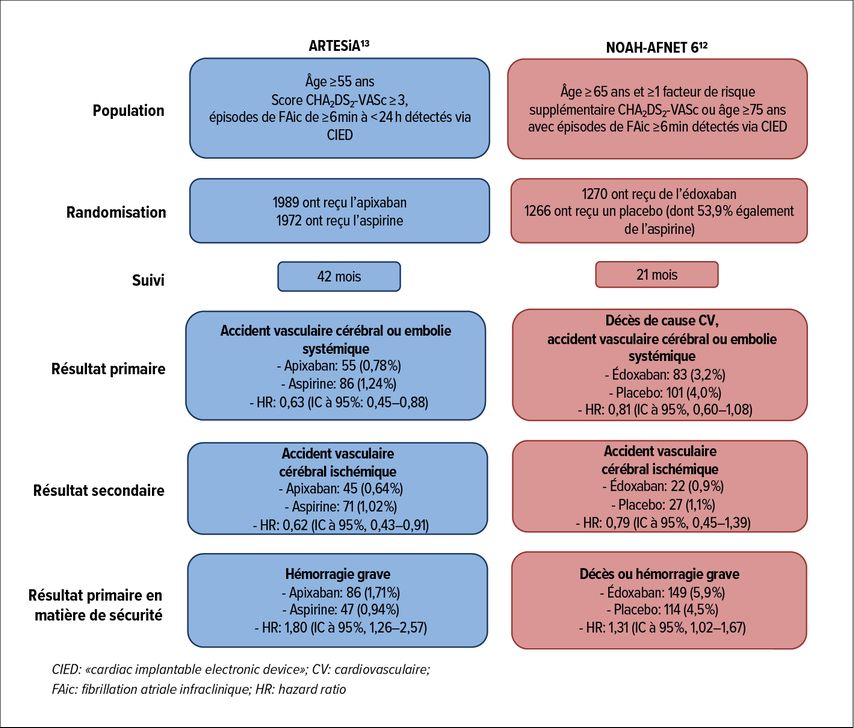
Deux grandes études randomisées sur le rôle des AOD dans les DDAF ont été publiées récemment (Tab. 1, Fig. 2).
Fig. 2: Aperçu des études randomisées et contrôlées sur l’utilisation d’anticoagulants oraux en cas de fibrillation atriale infraclinique. Les résultats sont exprimés en nombre de patients avec événement (%/année-patient) (adaptée de Svennberg E: N Engl J Med 2024; 390: 175-7)
Dans l’étude NOAH-AFNET 6, 2536 personnes présentant des DDAF ont été randomisées pour recevoir de l’édoxaban ou un placebo.12 Il est important de noter que plus de la moitié des patients du groupe placebo prenaient également de l’aspirine. Le critère d’évaluation primaire de l’étude était le décès d’origine cardiovasculaire, l’AVC ou l’ES. Après une période de suivi moyenne de 21 mois, l’étude a été arrêtée prématurément en raison de problèmes de sécurité et de l’évaluation d’une efficacité insuffisante. À la fin de l’étude, le critère d’évaluation primaire était apparu chez 3,2% des patients du groupe sous traitement actif et 4% du groupe placebo (HR: 0,81; p=0,15). Dans les deux groupes, l’incidence des AVC était très faible, avec respectivement 0,9 et 1,1% par patient-année. Le critère composite de sécurité comprenant la mortalité totale et les hémorragies graves s’est produit chez 5,9% des patients du groupe édoxaban et chez 4,5% des patients du groupe placebo (HR: 1,31; p=0,03), en raison d’un taux 2 fois plus élevé d’hémorragies graves mais non fatales, la mortalité totale ne différant pas entre les groupes.
Dans l’étude ARTESiA, 4012 patients présentant des DDAF d’une durée comprise entre 6 minutes et 24 heures ont été randomisés pour recevoir soit de l’apixaban, soit de l’aspirine.13 Dans les cas où la FA persistait plus de 24 heures ou évoluait vers une FA clinique, les médicaments de l’étude étaient arrêtés et une ACO était commencée. Au cours de la période de suivi moyenne de 3,5 ans, le critère d’évaluation primaire (AVC ou ES) est survenu chez 55 patients sous apixaban et 86 patients sous aspirine (0,78% vs 1,24% par patient-année; HR: 0,63; p=0,007). Les hémorragies graves étaient plus fréquentes sous apixaban (HR: 1,81; p=0,04). Cependant, aucune différence significative n’a été observée en ce qui concerne la survenue d’hémorragies fatales ou d’hémorragies intracrâniennes symptomatiques.
Une méta-analyse publiée récemment par les consortiums ARTESiA et NOAH-AF14 a ensuite confirmé de manière cohérente que l’ACO entraînait une réduction du risque relatif d’AVC de 32% (réduction du risque absolu de 1,2%), augmentait le risque relatif d’hémorragie grave de 62% (augmentation du risque absolu de 1,6%) et n’avait aucun effet sur la mortalité cardiovasculaire ou totale.
Heureusement, le taux annuel d’AVC est donc très faible (environ 1%). Il convient toutefois de noter que l’incidence des AVC invalidants à mortels (échelle de Rankin modifiée entre 3 et 6) a été réduite de moitié sous apixaban. Parallèlement, les hémorragies graves sous apixaban ont pu être traitées de manière conservatrice dans 90% des cas.
La sélection des patients est essentielle
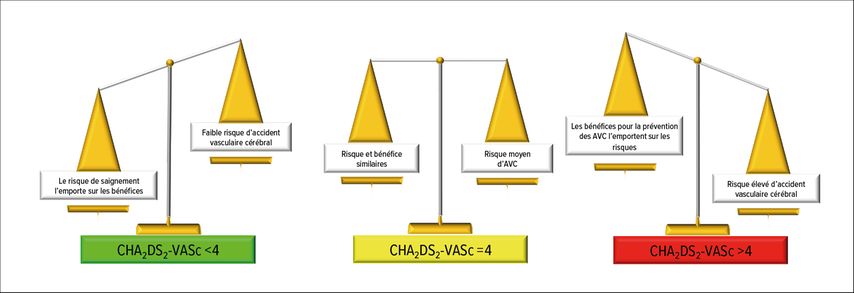
Les informations fournies par les deux essais contrôlés randomisés sont fondamentales pour une prise de décision fondée sur des preuves chez les patients présentant des DDAF. Les résultats de différentes sous-analyses des deux études peuvent donner quelques indications sur les facteurs qui pourraient être liés au risque d’accident vasculaire cérébral. Une sous-analyse de l’étude ARTESiA15 a montré que ni la fréquence ni la durée de l’épisode de DDAF le plus long ne modifiaient le risque d’AVC ou le bénéfice du traitement par apixaban. De la même manière, la cohorte NOAH a montré que la durée de la DDAF n’avait aucune influence sur l’efficacité et la sécurité de l’anticoagulation,16 alors que l’âge avancé, le diabète et la fonction rénale réduite étaient des prédicteurs importants de thromboembolies et d’hémorragies.17 Une sous-analyse de l’étude ARTESiA18 publiée en mai 2024 par Lopes et al. a montré que chez les patients ayant un score CHA2DS2-VASc >4, le taux d’AVC/ES était de 0,98% par an sous apixaban et de 2,25% par an sous aspirine. Dans ce sous-groupe, l’apixaban a évité 1,28 AVC/ES pour 100 patients-années sur une période de 3,5 ans et a provoqué 0,68 hémorragies majeurs par rapport à l’aspirine, l’augmentation des hémorragies n’étant pas statistiquement significative. Chez les patients ayant un score CHA2DS2-VASc >4, le «number needed to treat» pour un bénéfice à 3,5 ans était de 25 pour prévenir 1 AVC/ES, et le «number needed to harm» pour provoquer 1 hémorragie majeure était de 59. Les auteurs ont conclu que ces patients à très haut risque devraient être traités par des AOD, car ceux-ci semblent prévenir presque deux fois plus d’AVC/ES par rapport aux hémorragies graves. Chez les patients ayant un score CHA2DS2-VASc <4, il est peu probable que les patients bénéficient de l’ACO, car ils présentent un faible risque d’AVC et ce traitement provoque plus d’hémorragies graves qu’il ne prévient d’AVC/ES. Il existe un groupe intermédiaire considérable (CHA2DS2-VASc=4) pour lequel les préférences du patient peuvent aider à la décision de traitement (Fig. 3).
Fig. 3: Évaluation du rapport bénéfice/risque dans le traitement de la fibrillation atriale détectée via un appareil avec l’apixaban selon le score CHA2DS2-VASc (adaptée de Lopes RD et al., 2024)18
Conclusion
En cas de FA détectée via un appareil (DDAF), il n’est actuellement pas possible de donner une recommandation générale concernant le début d’une ACO. Chez des patients sélectionnés, notamment ceux présentant un risque individuel élevé d’AVC (CHA2DS2-VASc >4), l’utilisation d’un AOD peut être envisagée en tenant compte du bénéfice clinique net escompté et des préférences informées des patients. En outre, étant donné qu’environ un quart des patients développeront une FA clinique (durée >24h) dans les trois années suivantes, il est conseillé de surveiller plus étroitement les patients présentant des DDAF.
Littérature:
1 Van Gelder IC et al.: Eur Heart J 2024; 45: 3314-3414 2 Toennis T et al.: Europace 2023; 25: euad166 3 Hart RG et aI.: Ann Intern Med 2007; 146: 857-67 4 Ruff CT et al.: Lancet 2014; 383: 955-62 5 Eckman MH et al.: Circ Cardiovasc Qual Outcomes 2011; 4: 14-21 6 Glotzer TV et al.: Circ Arrhythm Electrophysiol 2009; 2: 474-80 7 Heale JS et al.: N Engl J Med 2012; 366: 120-9 8 Rahimi K: Eur Heart J 2017; 38: 1345-7 9 Svendsen JH et al.: Lancet 2021; 398: 1507-16 10 Lopes RD et al.: J Am Coll Cardiol 2024; 29: S0735-1097 11 Kemp Gudmundsdottir K et al.: Circulation 2024; doi: 10.1161/CIRCULATIONAHA.124.071176 12 Kirchhof P et al.: N Engl J Med 2023; 389: 1167-79 13 Healey JS et al.: N Engl J Med 2024; 390: 107-17 14 McIntyre WF et al.: Circulation 2024; 149: 981-8 15 McIntyre WF et al.: Circulation 2024; doi: 10.1161/CIRCULATIONAHA.124.069903 16 Becher N et al.: Eur Heart J 2024; 45: 837-49 17 Lip GYH et al.: Eur Heart J 2024; 45: 1733-7 18 Lopes RD et al.: J Am Coll Cardiol 2024; 84: 354-64