Stratégies thérapeutiques du cancer de la prostate hormono-dépendant
Auteur:
PD Dr méd. Aurelius Omlin
Onkozentrum Zürich und Chairman Uroonkologisches Zentrum, Hirslanden Zürich
E-mail: aurelius.omlin@ozh.ch
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
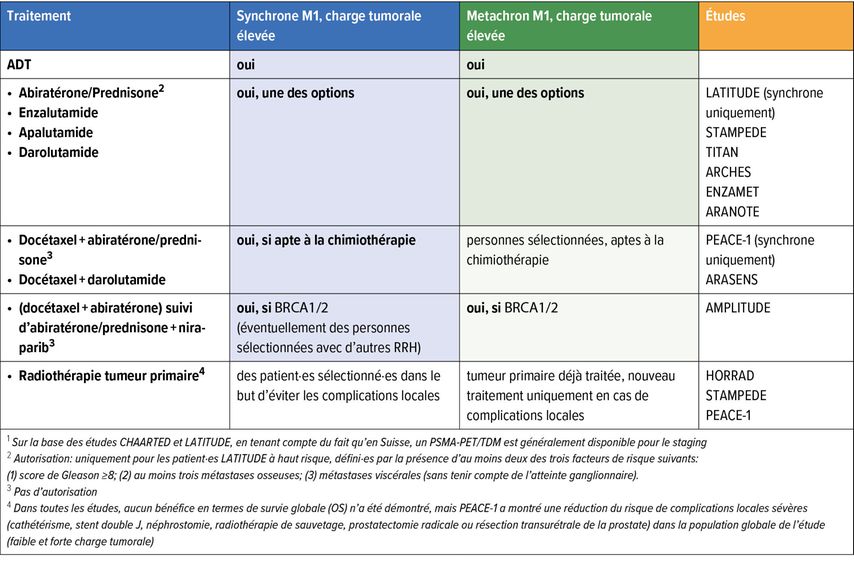
Le paysage thérapeutique du cancer de la prostate avancé a évolué et s’est enrichi presque chaque année depuis 2014 et la première présentation de l’étude CHAARTED. Aujourd’hui, les options thérapeutiques disponibles sont nombreuses et efficaces.
Chez les personnes atteintes d’un cancer de la prostate présentant une récidive biochimique après un traitement local (prostatectomie radicale ou radiothérapie), une élévation du taux de PSA constitue souvent un signal d’alarme ou un motif d’inquiétude.
Le standard dans cette situation est, après prostatectomie, une radiothérapie de sauvetage de la loge prostatique, avec ou sans irradiation du drainage lymphatique pelvien, et avec ou sans traitement de déprivation androgénique (ADT) supplémentaire – par exemple pendant 4 à 6 mois comme dans l’étude SPPORT ou 6 à 24 mois comme dans l’étude RADICALS. La méta-analyse DADSPORT a montré un net avantage en termes de survie sans métastases pour une durée courte ou longue d’hormonothérapie associée à la radiothérapie de sauvetage, ainsi qu’une tendance en faveur d’une durée plus longue de l’hormonothérapie pour la survie globale.1
Étude EMBARK
Pour les personnes présentant une récidive biochimique après traitement local d’un carcinome de la prostate, après un éventuel traitement local de sauvetage, et présentant un risque élevé de métastatisation (temps de doublement du PSA ≤9 mois et PSA ≥1 après prostatectomie ou ≥2 après radiothérapie), l’étude EMBARK a montré un avantage significatif en termes de survie sans métastases pour la combinaison ADT + enzalutamide vs ADT seule, ainsi que pour la monothérapie par enzalutamide vs ADT.
Lors du congrès européen sur le cancer ESMO 2025, les données de survie globale seront présentées à la mi-octobre. Selon le communiqué de presse, elles montrent également un avantage de survie significatif pour l’association ADT+enzalutamide par rapport à l’ADT seule.
Il est important de noter que l’étude EMBARK a eu recours à une imagerie conventionnelle et non à l’imagerie basée sur la PSMA. Nous savons, grâce à des études récemment publiées, que dans une population répondant aux critères de l’étude EMBARK, il est possible d’identifier une récidive chez environ 80% des patient·es grâce à l’imagerie TEP-PSMA:2
-
env. 25% de récidives locales
-
env. 50% de métastases ganglionnaires régionales
-
env. 25% de métastases ganglionnaires plus distantes
-
env. 25% de métastases osseuses et de combinaisons
Néanmoins, les données de l’étude EMBARK restent essentielles et permettent d’envisager un traitement systémique efficace pour ces personnes. La question de savoir si, en cas d’une imagerie TEP-PSMA et de détection d’oligométastases, un traitement local supplémentaire des métastases est pertinent reste ouverte et sera discutée lors de l’Advanced Prostate Cancer Consensus Conference 2026 (www.apccc.org).
Étude AMPLITUDE
Pour les personnes atteintes d’un cancer de la prostate métastasé et hormonosensible (mHSPC), une nouvelle possibilité thérapeutique a été présentée avec l’étude AMPLITUDE lors de l’ASCO 2025. Cette option peut être envisagée en cas d’altérations pertinentes des gènes impliqués dans la réparation par recombinaison homologue (BRCA1, BRCA2, BRIP1, CDK12, CHEK2, FANCA, PALB2, RAD51B, RAD54L).
Les personnes atteintes de mHSPC et présentant les altérations génomiques prédéfinies ont été randomisées dans l’étude pour recevoir ADT+abiratérone/prednisone ± l’inhibiteur de PARP niraparib. Un traitement antérieur par docétaxel pour mHSPC était autorisé et a été administré à 16% des participants. L’étude AMPLITUDE a montré un avantage cliniquement pertinent en survie sans progression radiologique pour l’association incluant l’inhibiteur de PARP, en particulier en présence chez les patient·esprésentant une altération BRCA1 ou BRCA2 (survie sans progression radiologique [rPFS]: non atteinte vs 26 mois; HR: 0,52; IC à 95%: 0,37–0,72). Dans la population totale de l’étude, cet avantage était également démontré (rPFS: non atteinte vs 29,5 mois; HR: 0,63; IC à 95%: 0,49–0,80).3
L’analyse des sous-groupes montre clairement que le bénéfice concerne surtout les altérations BRCA et probablement CHEK2. Pour les autres altérations, parfois peu représentées, il n’est pas possible de tirer des conclusions définitives.
Au moment de la présentation, aucun avantage significatif en survie globale n’a pu être démontré; des données complémentaires sont attendues au cours de l’étude. Il n’existe pour l’instant aucune autorisation de mise sur le marché pour cette combinaison thérapeutique, mais elle devrait être envisagée chez les personnes atteintes d’un cancer de la prostate métastatique présentant une altération BRCA1/2, notamment en cas de maladie métastatique synchrone et de charge tumorale élevée.
Remarque importante: si l’analyse moléculaire («next-generation sequencing», NGS) du tissu tumoral met en évidence l’une des altérations décrites dans l’étude AMPLITUDE, celle-ci doit être confirmée ou exclue dans la lignée germinale, une altération BRCA germinale ayant des implications importantes pour la personne concernée et sa famille dans le cadre d’une éventuelle prédisposition héréditaire au cancer.
PSMAddition & CAPItello-281
Au congrès ESMO 2025, deux autres études importantes portant sur la mHSPC seront présentées: PSMAddition, qui évalue l’apport supplémentaire d’une radioligandothérapie au 177Lutetium-PSMA-617 en association avec une ADT et un traitement endocrinien additionnel, comparativement à une combinaison endocrinienne seule.
Seront également présentées pour la première fois les données de l’étude CAPItello-281, qui évalue chez des personnes atteintes de mHSPC présentant une perte du gène suppresseur de tumeur PTEN le bénéfice additionnel de l’inhibiteur d’AKT, le capivasertib, en association avec abiratérone/prednisone+ADT, comparativement à l’ADT associée à abiratérone/prednisone+placebo. Selon le communiqué de presse, les deux études ont atteint leur critère d’évaluation primaire.
Conclusion
Nous pouvons nous attendre à une augmentation supplémentaire de la complexité dans le traitement des personnes atteintes d’un cancer de la prostate avancé, hormonosensible et métastasé. Ces données seront discutées avec les expert·es lors de la conférence de consensus 2026. Nous attendons avec intérêt les résultats des votes.
Les lignes directrices pourront intégrer et recommander les différentes options thérapeutiques efficaces, tandis que la conférence de consensus reflétera la manière dont un large comité international d’expert·es interprète les données actuelles et identifie d’éventuelles préférences pour l’une ou l’autre stratégie thérapeutique.
L’imagerie TEP-PSMA joue un rôle croissant dans le choix du traitement systémique (étude PSMAddition), et les marqueurs moléculaires (altérations HRR, perte de PTEN) permettent d’identifier des sous-groupes susceptibles de bénéficier d’approches ciblées.
Il reste essentiel de conseiller les personnes concernées et leurs proches de manière individualisée, en tenant compte des antécédents médicaux, des comorbidités, des traitements en cours, ainsi que des souhaits et objectifs de la personne concernée.
Littérature:
1 Burdett S et al.: Duration of androgen suppression with postoperative radiotherapy (DADSPORT) for nonmetastatic prostate cancer: a collaborative systematic review and meta-analysis of aggregate data. Eur Urol 2025; 88(3): 277-90 2 Holzgreve A et al.: PSMA-PET/CT findings in patients with high-risk biochemically recurrent prostate cancer with no metastatic disease by conventional imaging. JAMA Netw Open 2025; 8(1): e2452971 3 Attard G et al.: Phase 3 AMPLITUDE trial: niraparib (NIRA) and abiraterone acetate plus prednisone (AAP) for metastatic castration-sensitive prostate cancer (mCSPC) patients (pts) with alterations in homologous recombination repair (HRR) genes. J Clin Oncol 2025; 43(Suppl. 17): Abstr. #LBA5006
Das könnte Sie auch interessieren:
Infection par le VIH chez les personnes âgées: quels sont les défis?
Grâce aux progrès de la médecine, le VIH est aujourd’hui une maladie chronique qui peut être traitée et les patient·es peuvent avoir une espérance de vie presque normale. De plus en plus ...
Traitement par des anticorps dans la BPCO: premières autorisations et nombreuses questions en suspens
Les premiers médicaments biologiques ont désormais été autorisés dans l’indication de la BPCO pour réduire le risque d’exacerbation. Plusieurs autres médicaments biologiques font l’objet ...
Médicaments biologiques dans l’asthme sévère: l’embarras du choix
Pour le traitement de l’asthme bronchique sévère, six anticorps monoclonaux aux cibles différentes sont actuellement autorisés dans l’UE et en Suisse. Les biomarqueurs aident à choisir ...