Un traitement continu par ibrutinib est-il encore nécessaire en cas de LLC non traitée?
Compte-rendu:
Dre rer. nat. Ine Schmale
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
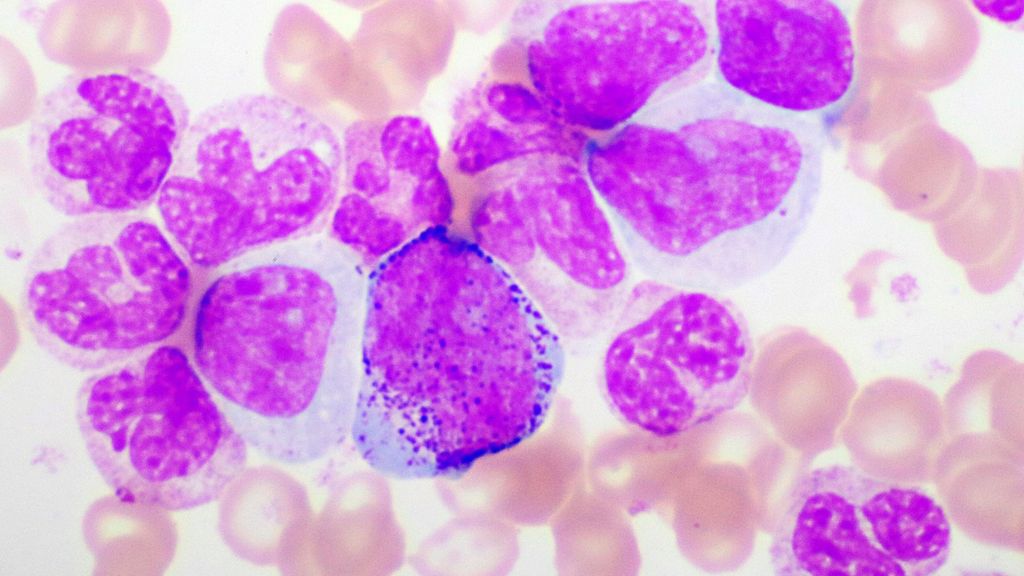
De nombreuses données d’études intéressantes sur la leucémie lymphoïde chronique (LLC) ont été présentées lors du congrès de l’ASH cette année. La question de savoir si un traitement continu par un inhibiteur de la tyrosine kinase de Bruton (BTKi) et un traitement à durée limitée associant le vénétoclax à un BTKi ou à un anticorps anti-CD20 sont comparables en termes d’efficacité a été évaluée dans le cadre randomisé de l’étude CLL17. Le BTKi non covalent pirtobrutinib a été comparé à l’ibrutinib dans l’étude face-à-face BRUIN CLL-314. L’étude FLAIR en cours évalue différents schémas thérapeutiques par rapport au schéma standard FCR chez des patient·es atteint·es de LLC en bon état général («fit»).
Le traitement à durée limitée constitue une bonne option pour les patient·es naïf·ves de traitement
Dans l’étude CLL17 à trois bras, des patient·es atteint·es de leucémie lymphoïde chronique (LLC) non traitée auparavant ont été randomisé·es (1:1:1) pour recevoir soit l’ibrutinib (420mg par jour jusqu’à progression), soit le vénétoclax (400mg par jour, 12 cycles) plus l’obinutuzumab (1000mg IV, 6 cycles), soit le vénétoclax (400mg par jour, cycles 4–15) plus l’ibrutinib (420mg par jour, 15 cycles). Au total, 909 patient·es ont été recruté·es entre février 2021 et novembre 2022. Les résultats, avec un suivi médian de 34,2 mois, ont été présentés en séance présidentielle sous forme d’abstract #1.1
L’âge médian des patient·es inclus·es était de 65 à 66 ans, et 43 à 44% étaient considéré·es comme «unfit». 56–57% des patient·es présentaient un statut IGHV non muté, 7–8% une mutation TP53/une délétion 17p, et environ 60% un risque élevé ou très élevé selon le score de l’International Pronostic Index (IPI) de la LLC.
Parmi les effets indésirables, les neutropénies sont à souligner: elles sont survenues chez 52,5% des patient·es dans le bras vénétoclax-obinutuzumab, 36,3% dans le bras vénétoclax-ibrutinib et 16,4% dans le bras ibrutinib. Une fibrillation auriculaire a été rapportée chez 3,7% (vénétoclax-obinutuzumab), 12,5% (vénétoclax-ibrutinib) et 16,8% (ibrutinib) des patient·es. Les infections sont survenues avec une fréquence comparable sous les trois schémas (76,3%, 80,2% et 79,9%), de grade3–5 chez 34,9%, 25,1% et 24,8% des patient·es.
Une réponse a été observée chez 84,2%, 88,5% et 86% des patient·es dans les trois bras; toutefois, les rémissions complètes étaient plus fréquentes avec les schémas contenant du vénétoclax (51,5% et 46,2%) qu’avec l’ibrutinib (8,3%). Une maladie résiduelle minimale indétectable (uMRD; <10–4) dans le sang périphérique ou la moelle osseuse a été observée chez 73,3% et 62% des patient·es sous vénétoclax-obinutuzumab, 47,2% et 40,0% sous vénétoclax-ibrutinib, et chez aucun·e patient·e dans le bras ibrutinib. Aucune différence n’a été observée pour la survie sans progression (PFS), avec des taux à 3 ans de 81,1%, 79,4% et 81,0%. Dans les sous-groupes définis par des mutations spécifiques, aucune différence significative n’a été observée entre les traitements. Le taux d’OS à 3 ans était comparable: 91,5%, 96,0% et 95,7%.
Conclusion
Les combinaisons à durée limitée de vénétoclax-obinutuzumab et de vénétoclax-ibrutinib se sont révélées non inférieures à un traitement continu par ibrutinib en termes de PFS. Le risque infectieux demeure pertinent pour les trois médicaments, en particulier lors de l’utilisation d’anticorps anti-CD20.
Pirtobrutinib chez les patient·es naïf·ves de cBTKi en première et deuxième ligne
L’étude randomisée de phaseIII BRUIN CLL-314 a comparé le pirtobrutinib à l’ibrutinib chez des patient·es atteint·es de LLC, en première ligne comme en situation de maladie récidivante ou réfractaire.2 Le critère d’évaluation primaire était la non-infériorité du pirtobrutinib par rapport à l’ibrutinib en termes de taux de réponse dans la population en intention de traiter (ITT) ainsi que dans la population en situation récidivante/réfractaire. Le critère d’évaluation secondaire évaluait la supériorité du pirtobrutinib par rapport à l’ibrutinib concernant la PFS, également dans la population ITT et dans la population récidivante/réfractaire. Au total, 662 patient·es ont été inclus·es (population ITT), dont 330 et 325 ont reçu au moins une dose du traitement à l’étude. Les patient·es (population ITT) étaientâgé·es en moyenne de 67 ans et vivaient avec une LLC depuis une durée médiane de 5,62 et 5,26 ans respectivement. Environ deux tiers présentaient un IGHV non muté, un tiers une mutation TP53, et 34 à 40% un caryotype complexe. Les patient·es en situation récidivante/réfractaire avaient reçu en médiane un traitement antérieur. Le critère d’évaluation principal de l’étude a été atteint; des taux de réponse systématiquement plus élevés ont été observés sous pirtobrutinib comparativement à l’ibrutinib. Une réponse a été observée chez 87,0 vs 78,5% des patient·es de la population ITT, 92,9 vs 85,8% de la population naïve de traitement (n=225) et 84,0 vs 74,8% dans la population récidivante/réfractaire (n=437). La PFS dans la population ITT (selon l’évaluation des investigateur·rices) a atteint le seuil de signification avec un rapport de risque de 0,57 et un IC à 95% de 0,39–0,83 (p=0,0034). Après 18 mois, 86,9% vs 82,3% des patient·es étaient sans progression. Un comité indépendant a également évalué la PFS au sein de la population ITT, montrant une tendance en faveur du pirtobrutinib (HR: 0,75; IC à 95%: 0,53–1,07; p=0,118). Selon cette analyse, le taux de PFS à 18 mois était de 84,7% vs 80,2%. Chez les patient·es naïf·ves de traitement, le taux de PFS à 18 mois était de 95,3% vs 87,6% (HR: 0,24; IC 95%: 0,10–0,59; p=0,0007) et, en situation récidivante/réfractaire, de 81,7% vs 79,2% (HR: 0,73; IC 95%: 0,47–1,13; p=0,1563), selon le comité indépendant.
Avec une durée médiane de traitement de 20,5 mois sous pirtobrutinib et de 19,3 mois sous ibrutinib, un·e patient·e sous pirtobrutinib versus quatre sous ibrutinib a développé une transformation de Richter. Une modification de dose pour effets indésirables liés au traitement a été nécessaire chez 7,9% (pirtobrutinib) vs 18,2% (ibrutinib) des patient·es; un arrêt du traitement a été rapporté chez 9,4% vs 10,8% des patient·es. Une fibrillation ou un flutter auriculaire est survenu chez 2,4% (grade≥3: 0,9%) vs 13,5% (grade≥3: 4,0%) de l’ensemble des patient·es; chez les ≥75 ans, les taux étaient de 4,5% (grade≥3: 1,5%) vs 21,4% (grade≥3: 7,1%).
Conclusion
Cette étude en face-à-face a démontré la non-infériorité du pirtobrutinib par rapport à l’ibrutinib en termes de réponse chez des patient·es atteint·es de LLC naïf·ves de cBTKi (inhibiteur covalent de la tyrosine kinase de Bruton), tant dans la population ITT que dans la population récidivante/réfractaire. Un avantage en termes de PFS a été observé en faveur du pirtobrutinib, en particulier dans la cohorte des patient·es naïf·ves de traitement. Le pirtobrutinib a été bien toléré et associé à de faibles taux de fibrillation ou de flutter auriculaire, y compris chez les patient·es âgé·es.
Amélioration du pronostic chez les patient·es à haut risque avec vénétoclax plus ibrutinib
L’étude de phaseIII multicentrique, randomisée et ouverte FLAIR inclut des patient·es atteint·es de LLC non traitée auparavant.3 Initialement, l’étude comparait l’ibrutinib plus rituximab (IR) au schéma FCR (fludarabine, cyclophosphamide, rituximab). Elle a ensuite été étendue aux bras ibrutinib plus vénétoclax (I+V) et ibrutinib seul (I). Au total, 1488 patient·es ont été inclus·es dans les quatre bras de l’étude. Chez 62% des patient·es, au moins une mutation était présente au début du traitement. Parmi l’ensemble, 36% présentaient un IGHV muté et 49,5% un IGHV non muté. Un réarrangement IGHV stéréotypé du sous-ensemble #2 (S#2) était observé chez 6,4% des patient·es, et le statut IGHV n’était pas disponible chez 8,1%. L’analyse a évalué l’impact des mutations présentes au début du traitement sur les taux de PFS et d’OS à 5 ans sous les différents traitements.
Chez les patient·es avec IGHV non muté, la PFS était significativement prolongée sous I+V par rapport aux bras combinés I et IR (HR: 0,2; IC 95%: 0,09–0,46; p<0,001) et par rapport au FCR (HR: 0,08; IC 95%: 0,03–0,17; p<0,001). Les taux de PFS à 5 ans étaient de 94,9%, 79,3% et 52,4%. Concernant l’OS, I+V a également montré les meilleurs succès thérapeutiques. Après 5 ans, 97,4% des patient·es sous I+V étaient en vie, contre 90,6% sous I ou IR et 88% sous FCR; 87% des patient·es du bras FCR ayant reçu en deuxième ligne un BTKi, du vénétoclax et parfois un anticorps anti-CD20. En cas de rémission complète MRD négative maintenue pendant une durée définie, le traitement de l’étude était interrompu et pouvait être repris en cas de MRD positive. 66% des patient·es sous I+V ont interrompu le traitement dans les 3 ans.
Le sous-groupe S#2 a également tiré le plus grand bénéfice du schéma I+V. Les taux de PFS à 5 ans étaient de 100% (I+V), 88,9% (I et IR) et 57,6% (FCR); les taux d’OS à 5 ans étaient de 100%, 90,9% et 86,7%. 60% des patient·es sous I+V ont arrêté le traitement en raison d’une MRD négative persistante dans les 3 ans. Un bénéfice significatif de I+V par rapport aux autres traitements a également été observé chez les patient·es présentant des aberrations ATM ou des mutations TP53, SF3B1 ou NOTCH1.
Chez les patient·es avec IGHV muté, la différence de PFS entre les bras de l’étude n’était significative que pour I+V vs FCR (HR: 0,47; IC à 95%: 0,24–0,89; p=0,021). L’OS était comparable entre les différents traitements dans ce sous-groupe. Après 5 ans, les taux de PFS étaient de 90,1%, 84,7% et 79%, et les taux d’OS de 92,2%, 92,1% et 92,4%.
Conclusion
Dans l’étude FLAIR, la thérapie ciblée par ibrutinib plus vénétoclax a significativement amélioré le pronostic des patient·es présentant un IGHV non muté, un S#2 ou des aberrations des gènes TP53, ATM ou NOTCH1. Environ deux tiers des patient·es à haut risque (dont la moitié avec mutation TP53) ont atteint une MRD négative et ont pu interrompre le traitement I+V dans les 3 ans.
Source:
Congrès annuel de l’American Society of Hematology (ASH) 2025, 6–9 décembre, Orlando, États-Unis
Littérature:
1 Al-Sawaf O et al.: Fixed-duration versus continuous targeted treatment for previously untreated chronic lymphocytic leukemia: results from the randomized CLL17 trial. ASH 2025; Abstr. #1 2 Woyach J et al.: Pirtobrutinib vs ibrutinib in treatment-naive and relapsed/refractory CLL/SLL: results from the first randomized phase III study comparing a non-covalent and covalent BTK inhibitor. ASH 2025; Abstr. #683 3 Dalal S et al.: MRD-guided ibrutinib plus venetoclax improves outcomes in CLL patients with TP53, ATM, or NOTCH1 aberrations compared to ibrutinib and FCR: results from the phase III NCRI FLAIR trial. ASH 2025; Abstr. #679
Das könnte Sie auch interessieren:
Gérer les effets indésirables de manière ciblée: pratique selon les directives S3 et internationales
Les thérapies systémiques contre le cancer prolongent la survie et permettent de contrôler les maladies tumorales. Il est déterminant que les patient·es tolèrent bien le traitement. Cela ...
Mise à jour: comment éviter les transfusions?
Chez les patient·es à faible risqueatteint·es de syndromes myélodysplasiques (SMD), l’anémie nécessitant des transfusions constitue souvent le principal problème altérant la qualité de ...
La radiothérapie adjuvante à l’ère des thérapies systémiques modernes
La radiothérapie adjuvante demeure un élément central dans le traitement des tumeurs malignes cutanées, malgré les progrès réalisés avec les immunothérapies et les thérapies ciblées. ...