Vers une classification génomique
Auteure:
Prof. Dre méd. Sara C. Meyer, PhD
Inselspital
Universitätsspital Bern
E-mail: sara.meyer@insel.ch
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Les marqueurs génétiques jouent un rôle de plus en plus important dans l’évaluation du risque des patient·es atteint·es de myélofibrose et dans l’algorithme thérapeutique. Une série d’inhibiteurs de JAK2 a considérablement élargi l’éventail des options thérapeutiques.
Le tableau clinique de la myélofibrose (MF) se caractérise par une fibrose progressive de la moelle osseuse et une hématopoïèse extramédullaire. Les symptômes comprennent notamment de la fièvre, des sueurs nocturnes et des douleurs abdominales dues à la splénomégalie. En outre, les patient·es présentent une tendance accrue aux thromboembolies et aux hémorragies ainsi qu’un risque accru de transformation leucémique. Sur le plan clinique, le spectre s’étend de l’oligosymptomatique au très agressif, ce pour quoi la stratification du risque joue un rôle essentiel.
L’approche thérapeutique curative comprend l’allogreffe de cellules souches hématopoïétiques (allo-CSH), qui ne peut pas être réalisée chez tous/toutes les patient·es. Dans le cadre du traitement symptomatique, on utilise des inhibiteurs de JAK2, des substances stimulant l’érythropoïèse, des transfusions et d’autres stratégies.
Mutations augmentant le risque
Les marqueurs génomiques sont aujourd’hui de plus en plus utilisés pour l’évaluation des risques, car ils influencent le pronostic et, dans certaines situations, la réponse au traitement. Le caryotype est pris en compte dans le calcul du score DIPSS-plus, en plus des facteurs cliniques, ce qui permet de différencier les groupes de pronostic avec une survie médiane de 1,3 à 15ans.1
Des mutations dans les gènes ASXL1, EZH2, SRSF2 et IDH1/2 ont été identifiées comme des altérations à haut risque et sont désormais aussi intégrées dans le score MIPSS70+.2 Une détection positive est corrélée à une réduction de la survie globale et à un risque accru de transformation.3 En relation avec la mutation TP53, la quantité joue un rôle important: ici, ce sont surtout les lésions «multi-hit» dans la phase chronique de la maladie qui ont un effet défavorable sur la probabilité de survie.4
Une classification génomique n’est pas encore une réalité aujourd’hui, mais les lignes directrices actualisées de l’EBMT/ELN sur l’allo-CSH en relation avec la MF intègrent des informations génétiques.5 Selon ces lignes directrices, l’allo-CSH est recommandée en cas de risque élevé ou de risque intermédiaire 2 selon le score DIPSS-plus et de risque élevé selon le score MIPSS70, en particulier en présence de cytopénies, d’une augmentation du nombre de blastes ou de mutations défavorables/d’une cytogénétique défavorable.
Grâce à des régimes de conditionnement mieux tolérés, l’âge moyen des patient·es atteint·es de NMP ayant subi une allo-CSH n’a cessé d’augmenter depuis l’an 2000.6 Les prétraitements par inhibiteur de JAK2 ont permis de réduire la taille moyenne de la rate avant l’intervention. Les mutations de JAK2, CALR et MPL sont considérées comme des aberrations significatives. Leur disparition 30jours après l’allo-CSH s’est avérée prédictive d’une diminution du risque de récidive.7
Anciens et nouveaux inhibiteurs de JAK2
Les patient·es pour lesquel·les l’allo-CSH n’est pas envisageable peuvent bénéficier des inhibiteurs de JAK2 de typeI comme le ruxolitinib, le momelotinib, le fedratinib et le pacritinib. Ces substances inhibent aussi bien la mutation de JAK2 que le type sauvage de JAK2 et sont actives dans la MF à mutation de JAK2, CALR et MPL, mais aussi dans la MF triplement négative.8,9 Le pacritinib n’a été autorisé qu’aux États-Unis, mais il est disponible en Suisse dans le cadre de programmes d’accès précoce. Le fedratinib a malheureusement récemment perdu son autorisation de mise sur le marché conditionnelle en Suisse.
Le ruxolitinib est utilisé depuis plus de dix ans comme inhibiteur de JAK «standard». La substance s’est avérée efficace pour contrôler les symptômes ainsi que réduire la taille de la rate, et elle apporte un avantage modéré en termes de survie.10 Il faudrait initier le traitement rapidement après la pose du diagnostic, car on peut alors s’attendre à des avantages significatifs dans le domaine de l’anémie et de la splénomégalie, qui peuvent se traduire par une survie globale prolongée.11
Une proportion substantielle de patient·es doit interrompre le traitement par ruxolitinib au bout de quelques années en raison d’une perte de réponse, d’effets secondaires ou d’une transformation leucémique, ce qui implique la nécessité d’un traitement de suivi, par exemple avec d’autres inhibiteurs de JAK2.12
Traitement des cytopénies
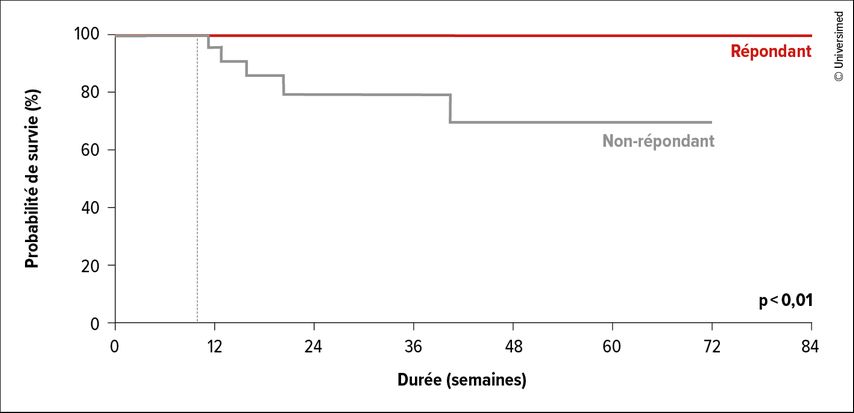
La MF accompagnée de cytopénies est fréquente dans la pratique clinique et difficile à traiter. Les directives du NCCN recommandent le momelotinib et le pacritinib pour la prise en charge de l’anémie associée à la MF.13 Le momelotinib a démontré une efficacité élevée en termes de réduction de l’anémie et de la dépendance transfusionnelle.14 Le pacritinib a entraîné une réduction solide de la splénomégalie, même en cas de thrombocytopénie et d’anémie sévères.15 Dans l’étude PERSIST-2, on a observé chez les patient·es thrombocytopéniques une corrélation entre la réponse à la splénomégalie sous pacritinib à trois mois et la survie globale (Fig. 1), ce qui n’a pas été observé sous le traitement de contrôle incluant le ruxolitinib (probablement en raison de réductions de dose).16
Fig.1: Corrélation entre la survie globale et la réponse au pacritinib (>10% de réduction de la splénomégalie; modifiée selon Ajufo H et al.)16
Dans les néoplasies myéloprolifératives, des inhibiteurs de JAK de typeII et JAK2V617F sélectifs sont en cours de développement clinique. La calréticuline mutée (CALR) comme cible ouvre l’option d’une thérapie basée sur l’immunologie sous forme d’anticorps monoclonaux ou bispécifiques. Une approche innovante consiste en l’utilisation de molécules de récepteurs de thrombopoïétine solubles ou de cellules CAR-T dirigées contre la CALR. Enfin, les cellules CAR-T peuvent également s’attaquer à la CALR.
L’optimisation du traitement de la MF devrait également être possible grâce à des thérapies combinées, dont plusieurs sont en cours d’évaluation clinique. Des études sont par exemple en cours sur l’inhibition de JAK2 en combinaison avec le ropeginterféron alfa-2b ou le pelabresib, un inhibiteur de BET. Ces résultats sont attendus avec impatience.
Littérature:
1 Gangat N et al.: DIPSS plus: a refined Dynamic International Prognostic Scoring System for primary myelofibrosis that incorporates prognostic information from karyotype, platelet count, and transfusion status. J Clin Oncol 2011; 29(4): 392-7 2 Tefferi A et al.: MIPSS70+ Version 2.0: Mutation and karyotype-enhanced International Prognostic Scoring System for primary myelofibrosis. J Clin Oncol 2018; 36(17): 1769-70 3 Vanucchi AM et al.: Mutations and prognosis in primary myelofibrosis. Leukemia 2013; 27(9): 1861-9 4 Tefferi A et al.: TP53 Mutations in myeloproliferative neoplasms: context-dependent evaluation of prognostic relevance. Am J Hematol 2025; 100(4): 552-60 5 Kröger N et al.: Indication and management of allogeneic haematopoietic stem-cell transplantation in myelofibrosis: updated recommendations by the EBMT/ELN International Working Group. Lancet Haematol 2024; 11(1): e62-74 6 Jungius S et al.: Characterization of engraftment dynamics in myelofibrosis after allogeneic hematopoietic cell transplantation including novel conditioning schemes. Front Oncol 2023; 13: 1205387 7 Gagelmann N et al.: Clearance of driver mutations after transplantation for myelofibrosis. N Engl J Med 2025; 392(2): 150-60 8 Rampal R et al.: Integrated genomic analysis illustrates the central role of JAK-STAT pathway activation in myeloproliferative neoplasm pathogenesis. Blood 2014; 123(22): e123-33 9 Szybinski J, Meyer SC: Genetics of myeloproliferative neoplasms. Hematol Oncol Clin North Am 2021; 35(2): 217-36 10 Al-Ali HK et al.: Primary analysis of JUMP, a phase 3b, expanded-access study evaluating the safety and efficacy of ruxolitinib in patients with myelofibrosis, including those with low platelet counts. Br J Haematol 2020; 189(5): 888-903 11 Verstovsek S et al.: Early intervention in myelofibrosis and impact on outcomes: apooled analysis of the COMFORT-I and COMFORT-II studies. Cancer 2023; 129(11): 1681-90 12 Harrison CN et al.: Fedratinib in patients with myelofibrosis previously treated with ruxolitinib: an updated analysis of the JAKARTA2 study using stringent criteria for ruxolitinib failure. Am J Hematol 2020; 95(6): 594-603 13 NCCN Guidelines Version 2.2024 Myelofibrosis 14 Harrison CN et al.: Longitudinal assessment of transfusion intensity in patients with JAK inhibitor-naive or -experienced myelofibrosis treated with momelotinib. Clin Lymphoma Myeloma Leuk 2025; 25(3): 199-211 15 Gagelmann N et al.: Consistency of spleen and symptom reduction regardless of cytopenia in patients with myelofibrosis treated with pacritinib. Clin Lymphoma Myeloma Leuk 2024; 24(11): 796-803 16 Ajufo H et al.: Pacritinib response is associated with overall survival in myelofibrosis: PERSIST-2 landmark analysis of survival. Eur J Haematol 2025; 114(2): 238-47
Das könnte Sie auch interessieren:
L’asthme et le rythme circadien
Le rythme circadien ne joue pas seulement un rôle important dans le sommeil, il a également une influence considérable sur les crises d’asthme et la fonction pulmonaire. Le ciblage ...
Technologies avancées et existantes dans la gestion du diabète
Même si le terme «traitement» est compris dans le nom de la conférence, la 18th International Conference on Advanced Technologies & Treatments for Diabetes (ATTD) constitue le rendez- ...
Les défis du diabète de type 1
Dans le cas du diabète de type 1, surtout s’il ne se déclare qu’à l’âge adulte, la pose du diagnostic peut déjà constituer un défi. Le risque d’hypoglycémie, qu’il faut minimiser, et le ...