Focus sur l’hypersomnolence
Auteur·es:
Dr méd. Hildegard Hidalgo1
Prof. Dr méd. Ulf Kallweit1,2
1 Zentrum für Narkolepsie und Hypersomnien, Stiftungsprofessur für Narkolepsie und Hypersomnolenzforschung
Fakultät für Gesundheit
Universität Witten/Herdecke
2 Centrum für seltene Schlaferkrankungen, CeSER – Centrum für seltene Erkrankungen Ruhr
E-mail: ulf.kallweit@uni-wh.de
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Environ 5 à 10% de la population générale sont concernés par des troubles de l’éveil. Ces troubles recouvrent un spectre large et incluent des manifestations fréquentes telles que la fatigue, la lassitude ou les troubles de l’attention. Les narcolepsies et les hypersomnies en constituent des causes plus rares de ces symptômes. Leur diagnostic et leur prise en charge sont présentés plus en détail ci-après.
Keypoints
-
L’hypersomnolence se caractérise par une somnolence diurne chronique et un besoin accru de sommeil. Elle doit être distinguée de la fatigue.
-
Les hypersomnolences primaires d’origine centrale comprennent les narcolepsies (types 1 et 2), l’hypersomnie idiopathique et l’hypersomnie périodique (syndrome de Kleine-Levin).
-
La narcolepsie de type 1 est associée à un déficit en orexine, probablement d’origine immunologique. Les causes des autres formes de narcolepsie et des hypersomnies restent en grande partie inconnues.
-
La prise en charge des hypersomnolences repose sur des mesures comportementales et une pharmacothérapie symptomatique.
Les hypersomnolences se caractérisent par une somnolence diurne, un besoin accru de sommeil et une incapacité à rester éveillé·e et cognitivement performant·e sur de longues périodes. Ce groupe d’affections touche environ 5 à 10% de la population.1
Parmi les causes les plus fréquentes figure la privation chronique de sommeil. L’hypersomnolence est également très fréquente dans le contexte de maladies neurologiques ou de la médecine interne et peut alors constituer la principale limitation fonctionnelle au quotidien. Elle peut aussi être associée à des troubles psychiatriques.
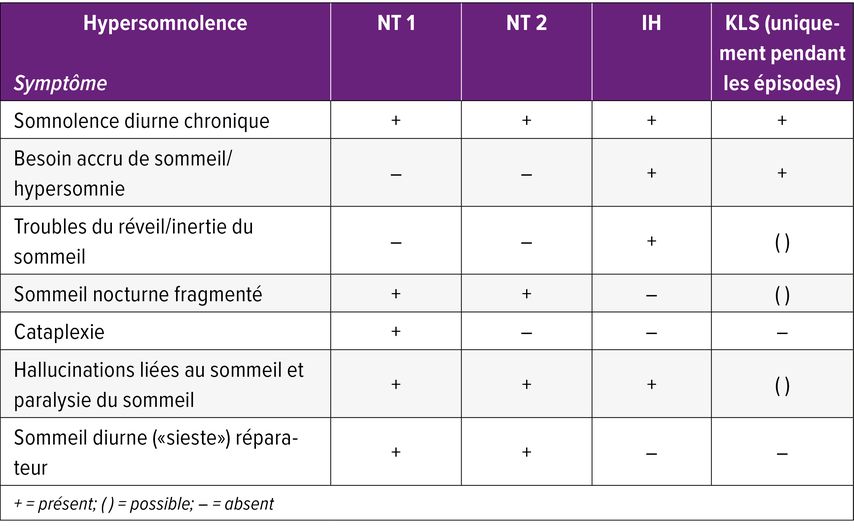
Lorsque l’hypersomnolence ne s’explique ni par une pathologie psychique ou somatique, ni par des effets médicamenteux, on parle de trouble central ou primaire avec hypersomnolence. La classification internationale des troubles du sommeil (ICSD-3-TR)2 distingue les hypersomnolences centrales en: narcolepsie de type1, narcolepsie de type2, hypersomnie idiopathique et hypersomnie périodique, également appelée syndrome de Kleine-Levin (voir Tab.1).
Narcolepsie de type1
La narcolepsie de type1 (NT1) présente une prévalence d’environ 20 à 50 personnes sur 1000003,4 et débute le plus souvent au cours de la deuxième décennie de la vie. Elle se caractérise par un besoin irrépressible de dormir, une somnolence chronique et une incapacité à maintenir un état de vigilance de qualité. Cet ensemble est généralement désigné comme somnolence diurne excessive («excessive daytime sleepiness» – EDS). Des cataplexies sont également observées. Il s’agit de brefs épisodes de perte bilatérale de tonus de certains groupes musculaires ou de l’ensemble de la musculature squelettique. Elles sont déclenchées par des émotions intenses, le plus souvent positives, sans altération de la conscience. D’autres symptômes peuvent être présents: sommeil nocturne fragmenté, cauchemars, rêves «intenses», hallucinations à l’endormissement ou au réveil (hallucinations hypnagogiques et hypnopompiques). Des paralysies du sommeil peuvent survenir lors de la transition entre le sommeil et l’éveil, les personnes concernées étant incapables de bouger malgré un état de conscience conservé. Ces cinq manifestations constituent la pentade de la narcolepsie.4
La diminution de la vigilance s’accompagne fréquemment de troubles de la concentration et de la mémoire ainsi que d’un épuisement généralisé, souvent non amélioré par un sommeil supplémentaire. Des comorbidités telles que la dépression ou les troubles anxieux sont fréquentes. L’intensité des symptômes varie et peut entraîner une atteinte marquée des activités de la vie quotidienne.3,4
La NT1 est causée par la destruction des neurones producteurs d’orexine au niveau de l’hypothalamus. Ces neurones jouent un rôle clé dans le maintien de l’éveil et la stabilisation des états d’éveil, de sommeil non-REM et de sommeil REM. Une association >95% de la maladie est observée avec l’haplotype HLA-DQB1*06:02.5 Ces éléments soutiennent l’hypothèse d’un mécanisme auto-immun à l’origine de la destruction neuronale.4,6,7 Selon une théorie, des agents infectieux induiraient un mimétisme moléculaire déclenchant une réponse immunitaire cellulaire et humorale dirigée contre certains épitopes neuronaux. Des liens entre certaines vaccinations et l’apparition de la narcolepsie de type1 ont également été rapportés.4, 7, 8 Une autre hypothèse évoque une dérégulation des lymphocytes T régulateurs, normalement chargés d’éliminer les cellules immunitaires autoréactives.7
Le diagnostic de la NT1 repose, selon les critères ICSD-3-TR, sur la présence d’une somnolence diurne chronique associée à des cataplexies. La somnolence diurne et sa sévérité peuvent être évaluées subjectivement à l’aide de questionnaires standardisés, tels que l’Epworth Sleepiness Scale (ESS). La Swiss Narcolepsy Scale constitue également un outil de dépistage utile.9
Avant toute exploration complémentaire, une privation chronique de sommeil doit être exclue à l’aide d’un agenda du sommeil et d’une actimétrie. Les médicaments sédatifs ou l’usage de substances psychoactives peuvent également être à l’origine d’une somnolence diurne chronique. Une imagerie cérébrale par résonance magnétique peut s’avérer nécessaire dans le cadre du diagnostic différentiel.
L’objectivation de la somnolence diurne et la confirmation diagnostique de la NT1 nécessitent une évaluation spécialisée comprenant une polysomnographie nocturne («Polysomnography», PSG) suivie d’un test itératif de latence d’endormissement («Multiple Sleep Latency Test», MSLT). Une latence moyenne d’endormissement inférieure à 8 minutes et la présence de plus d’une phase REM d’endormissement («Sleep Onset REM phase», SOREM) au cours du MSLTsont évocatrices. La mise en évidence d’une SOREM lors de la polysomnographie nocturne satisfait également aux critères diagnostiques. À titre alternatif, un taux d’orexine abaissé dans le liquide céphalorachidien (<110pg/ml) permet de poser un diagnostic certain.2
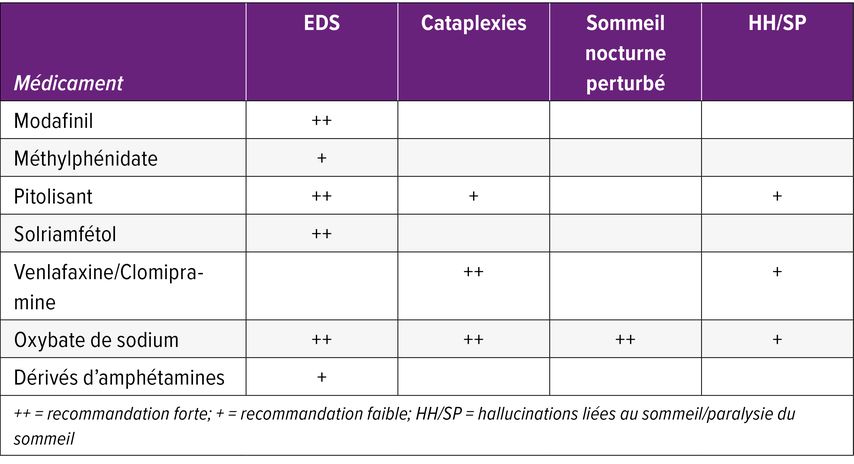
Sur le plan thérapeutique, la prise en charge associe des mesures comportementales de base – horaires de sommeil réguliers, courts épisodes de sommeil diurne planifiés de 10 à 20 minutes (siestes), activité physique et alimentation pauvre en glucides – et, le plus souvent, un traitement médicamenteux. Les traitements sont essentiellement symptomatiques et adaptés aux manifestations prédominantes. La somnolence diurne est traitée par des stimulants agissant principalement sur les voies nerveuses dopaminergiques, histaminergiques, adrénergiques et glutaminergiques. Les cataplexies peuvent être traitées par oxybate de sodium, pitolisant ou certains antidépresseurs, tels que la clomipramine et la venlafaxine (voir Tab.2).10 Compte tenu du déficit en orexine caractéristique de la NT1, plusieurs agonistes des récepteurs de l’orexine ont été développés ces dernières années et ont montré, à ce jour, des résultats très prometteurs.11
Tab. 2: Pharmacothérapie des narcolepsies chez l’adulte, adapté d’après Bassetti, Kallweit et al. 202110
Narcolepsie de type 2
La prévalence de la narcolepsie de type2 (NT2) n’est pas clairement établie. Aux États-Unis, elle est décrite plus fréquemment que la narcolepsie de type1, tandis qu’en Europe et en Asie, on estime généralement un rapport d’au moins 2:1 en faveur de la NT1 par rapport à la NT2. Les patient·es présentent une somnolence diurne marquée et rapportent, à des degrés variables, des hallucinations hypnagogiques ou hypnopompiques, un sommeil nocturne fragmenté ainsi que des paralysies du sommeil. Comparativement à la NT1, les symptômes sont toutefois souvent moins sévères. Chez environ 50% des patient·es, l’haplotype HLA-DQB1*06:02 est détectable; le taux d’orexine est quant à lui normal ou intermédiaire.4
Le diagnostic de NT2 repose sur le plan clinique, caractérisée par une somnolence diurne chronique, et sur les investigations en médecine du sommeil, incluant la PSG et le MSLT (voir ci-contre).2 Un petit nombre de patient·es développe, au cours de l’évolution, un déficit en orexine et des cataplexies, conduisant au diagnostic de NT1. À ce jour, les mécanismes physiopathologiques de la NT2 restent largement inconnus. Il est probable que la NT2 présente un tableau clinique hétérogène, reposant sur des mécanismes physiopathologiques eux-mêmes hétérogènes. Sur le plan thérapeutique, en plus des mesures comportementales (voir ci-contre), un traitement médicamenteux par médicaments favorisant l’éveil ou stimulants est généralement nécessaire10 (voir Tab.2).
Hypersomnie idiopathique
L’hypersomnie idiopathique (IH) est un trouble très rarement diagnostiqué. Dans l’entourage familial des patient·es, environ un tiers présente également une hypersomnolence, suggérant l’existence d’une prédisposition génétique.12 Cliniquement, l’IH se manifeste par une somnolence diurne chronique et, de manière subjective, par un sommeil nocturne souvent non réparateur, malgré une durée de sommeil prolongée dépassant généralement 10 heures. Les patient·es souffrent fréquemment d’un «trouble du réveil», caractérisé par l’incapacité à percevoir plusieurs alarmes ou même des sollicitations verbales directes, ainsi que d’une inertie du sommeil avec un réveil très laborieux. Cette inertie peut persister plusieurs heures. S’y ajoutent des troubles de la concentration («brain fog»), des altérations des capacités motrices et de la réactivité. De nombreuses personnes concernées décrivent le sentiment de ne jamais être pleinement éveillées au cours de la journée. Les siestes diurnes sont souvent prolongées (>1 heure) et non réparatrices. Des hallucinations hypnagogiques ou hypnopompiques peuvent survenir, et plus rarement des paralysies du sommeil. Le sommeil nocturne n’est interrompu que dans de rares cas.12
Différentes formes d’IH, avec durée de sommeil long ou normale, sont actuellement discutées. Sur le plan diagnostique, il est indispensable d’exclure les autres causes d’hypersomnolence. En polysomnographie, la confirmation du diagnostic requiert soit un temps total de sommeil (TST) d’au moins 660minutes, soit une latence moyenne d’endormissement de < 8 minutes lors du MSLT. L’actigraphie peut également contribuer à démontrer l’hypersomnie.2 La prise en charge repose sur des stimulants ou substances favorisant l’éveil, des antidépresseurs à effet activateur et, plus rarement, sur l’oxybate de sodium. Toutes ces options thérapeutiques sont utilisées hors indication («off-label») en Europe.
Différenciation entre NT2 et IH – «spectre de la narcolepsie»
Comme pour la NT2, aucun corrélat physiopathologique du trouble n’a pu être identifié à ce jour pour l’IH. Dans les deux cas, le diagnostic repose sur la clinique et les examens PSG/MSLT, la distinction s’appuyant essentiellement sur la présence ou l’absence de SOREM lors du MSLT. Toutefois, la sensibilité et la spécificité limitée du MSLT ont été rapportées à plusieurs reprises, rendant la délimitation entre ces tableaux cliniques parfois peu fiable en pratique clinique quotidienne et pouvant nécessiter la répétition des examens.13
Dans une étude de phénotypage guidée par les données, incluant plus de 1000 patient·es souffrant d’hypersomnolence, les patient·es atteint·es de NT1 ont pu être clairement regroupé·es au sein de clusters homogènes, contrairement aux patient·es présentant une NT2 ou une IH. Ces résultats suggèrent l’existence de bien plus de types ou sous-types que ceux actuellement reconnus.14 Un consensus croissant se dégage quant à la nécessité de faire évoluer la classification des hypersomnolences.15
Hypersomnie récurrente (syndrome de Kleine-Levin)
Le syndrome de Kleine-Levin (KLS) est une hypersomnie épisodique dont la prévalence estimée est de 1 à 5 cas par 1000 000.16
Il touche principalement des adolescents et de jeunes adultes de sexe masculin. Sur le plan clinique, on observe des épisodes de somnolence extrême, avec des durées de sommeil pouvant atteindre jusqu’à 18 heures par jour. Pendant les phases d’éveil, la vigilance est réduite et s’accompagne de dysfonctions cognitives, notamment de troubles de la mémoire (en particulier mémoire de travail et mémoire déclarative), ainsi que d’apathie. Des troubles du comportement alimentaire (anorexie ou hyperphagie), des troubles du contrôle des impulsions (p. ex. hypersexualité) et des phénomènes de déréalisation sont fréquemment associés. Une amnésie partielle ou complète des épisodes est souvent rapportée a posteriori. Les épisodes durent généralement une à quatre semaines et se répètent à des intervalles variables, le plus souvent au moins une fois tous les 12 à 18 mois.16 Entre les épisodes, l’attention, les fonctions cognitives, le comportement et l’humeur sont entièrement préservés. Les personnes concernées sont alors parfaitement «normales». La pathogenèse de la maladie reste inconnue. Les hypothèses évoquées incluent des troubles du développement, des mécanismes immunologiques ou encore une variation génétique du locus TRANK1.17 Le diagnostic est établi selon les critères ICSD-3-TR2, sur la base de la symptomatologie clinique, avec la survenue d’au moins deux des épisodes mentionnés ci-dessus. +Les autres causes, y compris les troubles psychiatriques, doivent être rigoureusement exclues dans le diagnostic différentiel. Chez la grande majorité des personnes concernées, les épisodes – et donc la maladie – cessent spontanément après 10 à 20 ans. Les approches thérapeutiques visent principalement à assurer un environnement sécurisé pendant les épisodes et à maintenir un rythme veille-sommeil régulier, avec des durées de sommeil suffisantes en dehors des phases aiguës. Dans des cas isolés, un allongement des intervalles entre les épisodes a été rapporté sous traitement prophylactique de phase, notamment par lithium, carbamazépine, valproate, phénytoïne ou phénobarbital.16
Littérature:
1 Ohayon MM: From wakefulness to excessive sleepiness: what we know and still need to know. Sleep Med Rev 2008; 12(2): 129-41 2 The AASM International Classification of Sleep Disorders – Third Edition. Text Revision (ICSD-3-TR). Westchester, IL: American Academy of Sleep Medicine; 2023 3 Kallweit U et al.: Prevalence, incidence, and health care utilization of patients with narcolepsy: a population-representative study. J Clin Sleep Med 2022; 18(6): 1531-7 4 Bassetti CLA et al.: Narcolepsy - clinical spectrum, aetiopathophysiology, diagnosis and treatment. Nat Rev Neurol 2019; 15(9): 519-39 5 Tafti M et al.: DQB1 locus alone explains most of the risk and protection in narcolepsy with cataplexy in Europe. Sleep 2014; 37(1): 19-25 6 Latorre D et al.: T cells in patients with narcolepsy target self-antigens of hypocretin neurons. Nature. 2018; 562(7725): 63-8 7 Kallweit U, Dittmar T: Pathophysiologie der Narkolepsie. Somnologie 2025; 29: 17-23 8 Hidalgo H et al.: Post tick-borne encephalitis virus vaccination narcolepsy with Cataplexy. Sleep 2016; 39(10): 1811-4 9 Bargiotas P et al.: The Swiss Narcolepsy Scale (SNS) and its short form (sSNS) for the discrimination of narcolepsy in patients with hypersomnolence: a cohort study based on the Bern Sleep-Wake Database. J Neurol 2019; 266(9): 2137-43 10 Bassetti CLA et al.: European guideline and expert statements on the management of narcolepsy in adults and children. Eur J Neurol 2021; 28(9): 2815-30 11Dauvilliers Y et al.: Oveporexton, an oral orexin receptor 2-selective agonist, in narcolepsy type 1. N Engl J Med 2025; 392(19): 1905-16 12 Billiard M, Sonka K: Idiopathic hypersomnia. Sleep Med Rev 2016; 29: 23-33 13 Trotti LM: Test-retest reliability of the multiple sleep latency test in narcolepsy without cataplexy and idiopathic hypersomnia. J Clin Sleep Med 2013; 9(8): 789-95 14 Gool JK et al.: Data-driven phenotyping of central disorders of hypersomnolence with unsupervised clustering. Neurology 2022; 98(23): e2387-e400 15 Lammers GJ et al.: Diagnosis of central disorders of hypersomnolence: a reappraisal by European experts. Sleep Med Rev 2020; 52: 101306 16 Arnulf I et al.: Diagnosis, disease course, and management of patients with Kleine-Levin syndrome. Lancet Neurol 2012; 11(10): 918-28 17 Ambati A et al.: Kleine-Levin syndrome is associated with birth difficulties and genetic variants in the TRANK1 gene loci. Proc Natl Acad Sci USA 2021; 118(12): e2005753118
Das könnte Sie auch interessieren:
Modèles prédictifs pour l’indication de la GPE chez les patient·es atteint·es de SLA
La gastrostomie percutanée endoscopique (GPE) est couramment utilisée dans la sclérose latérale amyotrophique (SLA) avancée. Le moment optimal de la mise en place fait toutefois l’objet ...
Mécanismes d’action de l’ECT en tant que traitement alternatif de la dépression
La dépression compte parmi les troubles psychiques les plus fréquents et les plus invalidants, mais ses fondements neurobiologiques ne sont à ce jour que partiellement élucidés. L’ ...
Psychothérapie augmentée à la kétamine
La (S-)kétamine, antidépresseur à action rapide, est utilisée de manière efficace chez les patient·es présentant une résistance aux traitements. Pour les doses subanesthésiques, on ...