Akute myeloische Leukämie (AML) – State of the Art 2025
Autor:
Dr. Gregor Eisenwort
3. Medizinische Abteilung
Hanusch-Krankenhaus, Wien
E-Mail: gregor.eisenwort@oegk.at
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Die aktuellen Therapiestandards der akuten myeloischen Leukämie ermöglichen eine spezifisch auf die Patient:innen abgestimmte Therapie, je nach Eignung für Chemotherapie und genetischem Risikoprofil. Während fitten Patient:innen mit intensiver Chemotherapie und gegebenenfalls allogener Stammzelltransplantation ein kurativer Therapieansatz angeboten werden kann, steht auch unfitten Patient:innen eine potente Behandlung durch die Kombination von hypomethylierenden Substanzen in Kombination mit Venetoclax oder spezifischen Inhibitoren zur Verfügung.
Keypoints
-
Die Eignung einer Patientin/eines Patienten für die intensive Therapie hängt von mehreren Faktoren ab, vor allem von Alter, Komorbiditäten sowie funktionellem und kognitivem Status.
-
Bei fitten Patient:innen besteht ein kurativer Therapieansatz in Form von intensiver Chemotherapie und je nach genetischem Profil Erweiterung um einen FLT3-Inhibitor oder Gemtuzumab-Ozogamicin. Bei intermediärem und hohem Risiko ist eine allogene Stammzelltransplantation anzustreben.
-
Unfitte Patient:innen können durch die Kombination von hypomethylierenden Substanzen und Venetoclax (bzw. bei IDH1-Mutation Ivosidenib) ebenso ein lang anhaltendes Therapieansprechen erreichen.
-
Neue Studien zu Kombinationstherapien und neuen Substanzklassen (v.a. Menin-Inhibitoren) und nichtintensiven Ansätzen auch bei fitten Patient:innen werden die therapeutische Landschaft der AML in den nächsten Jahren verändern.
Die akute myeloische Leukämie (AML) ist eine seltene und schwere hämatoonkologische Erkrankung, die unbehandelt rasch zum Tod führt. Die klinische Präsentation ist sehr heterogen und reicht von asymptomatischen Zufallsbefunden über extramedulläre Manifestationen (Gingivahyperplasie) bis hin zur schweren Sepsis. Laborchemisch wegweisend finden sich häufig eine Leukozytose oder eine Leukopenie in Kombination mit Anämie und/oder Thrombozytopenie und möglicherweise Blasten im Differenzialblutbild (wobei ein unauffälliges Blutbild eine AML nicht ausschließt).
Diagnostisches Kriterium ist ein Blastenanteil von über 20% im Knochenmark oder im peripheren Blut. Zur kompletten Diagnostik sollten im Rahmen einer Knochenmarkspunktion neben der Zytomorphologie auch Material zur Durchflusszytometrie und Gentestung (FiSH, Karyotyp, NGS) sowie eine Stanze für die histologische Aufarbeitung gewonnen werden.
Ist die Diagnose bestätigt, ist der nächste Schritt die Evaluierung der Therapiefitness. Hierbei spielen mehrere Faktoren eine Rolle. Neben dem Alter und bestehenden Komorbiditäten sind auch der funktionelle, der kognitive und der Ernährungstatus zu berücksichtigen. Letztlich spielen auch die allgemeine „Frailty“ (Gebrechlichkeit), die Versorgungssituation und natürlich der Patient:innenwunsch eine Rolle.1
Intensive Therapie
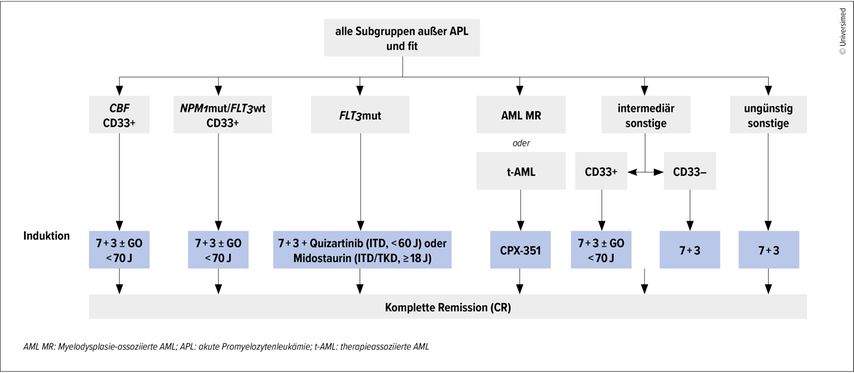
Bei Patient:innen, die fit für eine intensive Therapie sind, besteht grundsätzlich ein kurativer Therapieanspruch. Die genaue Therapie richtet sich dabei nach den zugrunde liegenden genetischen Veränderungen und der Risikostratifizierung des European Leukemia Net (ELN) (Abb. 1 und Tab. 1).2,3
Abb. 1: Therapie-Algorithmus für die initiale Entscheidung bei Erstdiagnose (modifiziert nach Onkopedia-Leitlinie AML)3
Tab. 1: Molekular-zytogenetische Risikogruppen gemäß der Klassifikation des ELN 2022 (modifiziert nach Döhner H und Onkopedia-Leitlinie AML)2,3
Rückgrat der Induktionstherapie ist in jedem Fall die Kombination eines Anthrazyklins mit Cytarabin, das sogenannte 3+7-Schema. Je nach genetischem Profil kann diese Therapie noch erweitert werden: Patient:innen mit einer „Core-binding factor“(CBF)-Mutation – inv(16) oder t(8:21) – oder mit Mutation im NPM-1-Gen profitieren von der Hinzunahme des Antibody-Drug-Konjugates (ADC) Gemtuzumab-Ozogamicin (GO).4 Bei Patient:innen, bei denen eine FLT3-Mutation vorliegt, ist ein oraler FLT3-Inhibitor (Midostaurin oder Quizartinib) hinzuzufügen.5,6 Patient:innen mit einer Hochrisikokonstellation nach ELN erhalten die Chemotherapie ohne weitere Ergänzungen.
Einen Sonderfall bilden Patient:innen, bei denen eine AML mit Myelodysplasieassoziierten Veränderungen vorliegt (zytogenetisch oder im NGS) oder bei denen bereits im Vorfeld ein myelodysplastisches Syndrom (MDS) diagnostiziert worden ist, sowie Patient:innen, die in der Vergangenheit bereits eine Chemotherapie aufgrund einer anderen onkologischen Erkrankung erhalten haben. In diesen Gruppen ist die Verwendung von CPX-351, einer liposomalen Fixkombination aus Daunorubicin und Cytarabin, empfohlen.7
Ziel der Induktionstherapie ist das Erreichen einer kompletten Remission (CR), also eines Blastenanteils von unter 5% im Knochenmark bei adäquat regeneriertem peripherem Blutbild und Rückbildung aller extramedullären Manifestationen.2 Ist die CR erreicht, können je nach Risikoprofil konsolidierende Therapien angeschlossen werden. Patient:innen mit hohem (und in den meisten Fällen auch solche mit intermediärem) Risiko nach ELN sollten bei Verfügbarkeit einer geeigneten Spenderin oder eines geeigneten Spenders auf jeden Fall für eine allogene Stammzelltransplantation evaluiert werden.8 Patient:innen mit niedrigem Risiko werden konsolidierend mit 4 Zyklen intermediär dosiertem Cytarabin konsolidiert.2
Zum Monitoring des Therapieansprechens über das Erreichen einer CR hinaus (sowie zum frühzeitigen Erkennen von Rezidiven) besteht die Möglichkeit der Messung der minimalen Resterkrankung (MRD) in Blut oder Knochenmark, im Falle einer CBF- oder NPM-1-Mutation mittels Real-time-PCR, in den meisten anderen Fällen mittels Durchflusszytometrie.2
Nichtintensive Therapie
Obwohl Patient:innen, die nicht fit für intensive Therapie sind, in den meisten Fällen keine kurativen Therapieoptionen zur Verfügung stehen, besteht auch bei diesem Kollektiv die Möglichkeit eines lang anhaltenden Therapieansprechens.
Therapie der ersten Wahl ist in den meisten Fällen die Kombination aus einer hypomethylierenden Substanz (HMA, Azacitidin oder Decitabin) und dem oralen BCL-2-Inhibitor Venetoclax.9 Unter dieser Kombination kommt es zu hohen Ansprechraten, wobei die Wahrscheinlichkeit des Ansprechens ähnlich wie bei den intensiven Therapien vom genetischen Profil abhängt. Die Risikostratifizierung unterscheidet sich hierbei allerdings von der intensiven Therapie (und ist in einer eigenen ELN-Risikostratifizerung für unfitte Patient:innen zusammengefasst)10: Kurz gesagt zeigen Patient:innen mit mutiertem TP53 ein schlechtes Ansprechen, während Mutationen in FLT3, NRAS oder KRAS (aber TP53-Wildtyp) ein intermediäres Ansprechen prognostizieren. Bei Patient:innen mit keiner der genannten Mutationen besteht eine günstige Risikokonstellation und sie profitieren am ehesten von der Kombination.
Ebenso sind Patient:innen mit IDH-1-Mutation als günstig einzustufen (ca. 5–10% der AML), da in dieser Gruppe die Kombination von Azacitidin mit dem IDH-1-Inhibitor Ivosidenib zur Verfügung steht.11 Die beiden Kombinationen sind nach den Leitlinien in diesem Fall gleichwertig, wobei in der Praxis bei Vorliegen einer IDH-1-Mutation häufig Azacitidin und Ivosidenib aufgrund der besseren Verträglichkeit bevorzugt werden.
Die beiden verfügbaren Kombinationstherapien sind jeweils mit einem eigenen Nebenwirkungsspektrum vergesellschaftet: Ivosidenib kann zu Verlängerungen der QTc-Zeit und einem möglichen Leukozytendifferenzierungssyndrom mit Flüssigkeitseinlagerungen und Pleuraergüssen führen. Unter der Therapie mit Venetoclax kommt es hingegen häufig zu Leuko- und Thrombopenien (zum Teil mit schweren Infektionen und/oder Blutungen), sodass die Regeldosis von 400mg über 28 Tage reduziert werden muss (wobei keine einheitlichen Richtlinien zur Dosisanpassung existieren). Dosisreduktionen sind bei ebenfalls gleichzeitiger Anwendung von CYP3A4-Inhibitoren (z.B. Azol-Antimykotika) vorzunehmen.12 Somit ist auch bei den nichtintensiven Therapien, vor allem in der Anfangsphase bis zum Erreichen einer CR, eine engmaschige klinische Beobachtung der Patient:innen geboten.
Patient:innen, die sich aufgrund einer besonders hohen „Frailty“ nicht für eine der genannten Kombinationstherapien eignen, können nach den Leitlinien auch mit einer HMA-Monotherapie behandelt werden.13
Die nichtintensiven Therapien werden auch bei Erreichen einer CR fortgesetzt, bis es zum Rezidiv bzw. Progress oder zu inakzeptabler Toxizität kommt, wobei in Einzelfällen (bei Patient:innen, deren Fitness sich unter der Therapie gebessert hat) eine allogene Stammzelltransplantation in CR eine kurative Option sein kann.
Ausblick
Die Therapielandschaft der AML wird sich in den kommenden Jahren voraussichtlich verändern. Zum einen wird die Substanzklasse der Menin-Inhibitoren an Bedeutung gewinnen: Menin ist ein Protein, das als Onkogen in Leukämien mit NPM-1-Mutation und/oder KMT2A-Umlagerung wirkt. Menin-Inhibitoren werden aktuell in klinischen Studien in verschiedenen Settings als Kombinationspartner mit intensiver Chemotherapie, als Erweiterung bei nichtintensiven Therapien oder auch in der Monotherapie getestet. Dabei umfassen die Studien sowohl neu diagnostizierte als auch rezidivierte/refraktäre Patient:innen. Bislang ist nur ein einziger Menin-Inhibitor, Revumenib, von der FDA zur Monotherapie im rezidivierten/refraktären Setting zugelassen, doch die Vielzahl an aktuell laufenden Studien wird höchstwahrscheinlich zu Neuzulassungen auch im europäischen Raum führen.14
Ein weiterer Trend, der in aktuellen Studien vermehrt zu bemerken ist, ist eine zunehmende Intensivierung der Therapieprotokolle im Sinne von Dreifachkombinationen. Insbesondere im Bereich der nichtintensiven Therapie wird derzeit die Kombination von HMA und Venetoclax mit gezielten Inhibitoren (je nach zugrunde liegender genetischer Veränderung FLT3, IDH-1 oder auch Menin) getestet.15
Zu guter Letzt mehrt sich in verschiedenen Studien Evidenz, dass auch Patient:innen, die grundsätzlich fit für eine intensive Therapie sind, unter gewissen Umständen von nichtintensiven Protokollen wie HMA plus Venetoclax profitieren (im Sinne vergleichbarer Effektivität bei geringerer Toxizität).16 Es ist vorstellbar, dass dies in der Zukunft zu einem Paradigmenwechsel hin zum vermehrten Einsatz der nichtintensiven Therapien auch bei fitten Patient:innen führen wird, falls sich diese Beobachtungen in groß angelegten Phase-III-Studien bestätigen.
Fazit
Die aktuellen Therapieleitlinien der AML erlauben eine individuelle Therapie, die sowohl an die genetischen Faktoren der jeweiligen Erkrankung als auch an patient:innenspezifische Faktoren in Bezug auf die Therapiefitness angepasst ist. Durch neue Substanzklassen wie Menin-Inhibitoren, neue Kombinationsregimes und den Einsatz nichtintensiver Protokolle bei fitten Patient:innen wird sich die Therapielandschaft in den nächsten Jahren weiter spezialisieren und verändern.
Literatur:
1 Venugopal S, Sekeres MA: Contemporary management of acute myeloid leukemia. JAMA Oncol 2024; 10(10): 1417-25 2 Döhner H et al.: Diagnosis and management of AML in adults: 2022 recommendations from an international expert panel on behalf of the ELN. Blood 2022; 140(12): 1345-77 3 Onkopedia-Leitlinie AML (Stand: September 2025): www.onkopedia.com/de/onkopedia/guidelines/akute-myeloische-leukaemie-aml 4 Lambert J et al.: Gemtuzumab ozogamicin for de novo acute myeloid leukemia: final efficacy and safety updates from the open-label, phase III ALFA-0701 trial. Haematologica 2019; 104(1): 113-9 5 Erba HP et al.: Quizartinib plus chemotherapy in newly diagnosed patients with FLT3-internal-tandem-duplication-positive acute myeloid leukaemia (QuANTUM-First): a randomised, double-blind, placebo-controlled, phase 3 trial. Lancet 2023; 401 (10388): 1571-83 6 Stone RM et al.: Midostaurin plus chemotherapy for acute myeloid leukemia with a FLT3 mutation. N Engl J Med 2017; 377(5): 454-64 7 Lancet JE et al.: CPX-351 (cytarabine and daunorubicin) liposome for injection versus conventional cytarabine plus daunorubicin in older patients with newly diagnosed secondary acute myeloid leukemia. J Clin Oncol 2018; 36(26): 2684-92 8 Cornelissen JJ et al.: The European LeukemiaNet AML Working Party consensus statement on allogeneic HSCT for patients with AML in remission: an integrated-risk adapted approach. Nat Rev Clin Oncol 2012; 9(10): 579-90 9 Pratz KW et al.: Long-term follow-up of VIALE-A: venetoclax and azacitidine in chemotherapy-ineligible untreated acute myeloid leukemia. Am J Hematol 2024; 99(4): 615-24 10 Döhner H et al.: Genetic risk classification for adults with AML receiving less-intensive therapies: the 2024 ELN recommendations. Blood 2024; 144(21): 2169-73 11 Montesinos P et al.: Long-term results from the AGILE study of azacitidine plus ivosidenib vs placebo in newly diagnosed IDH1-mutated AML. Blood Adv 2025; 9(20): 5177-89 12 Wei AH et al.: How I treat patients with AML using azacitidine and venetoclax. Blood 2025; 145(12): 1237-50 13 Kantarjian HM et al.: Multicenter, randomized, open-label, phase III trial of decitabine versus patient choice, with physician advice, of either supportive care or low-dose cytarabine for the treatment of older patients with newly diagnosed acute myeloid leukemia. JClin Oncol 2012; 30(21): 2670-7 14 Huls G et al.: Menin inhibitors in the treatment of acute myeloid leukemia Blood 2025; 145(6): 561-6 15 Venugopal S, Watts J: The future paradigm of HMA + VEN or targeted inhibitor approaches: sequencing or triplet combinations in AML therapy. Hematology 2023; 2023: 192-7 16 Lu J et al.: Venetoclax and decitabine vs intensive chemotherapy as induction for young patients with newly diagnosed AML. Blood 2025; 145(22): 2645-55
Das könnte Sie auch interessieren:
T-Prolymphozyten-Leukämie (T-PLL): Welche Entwicklungen gibt es?
Die seltene T-Prolymphozyten-Leukämie (T-PLL) zeichnet sich durch einen meist aggressiven Verlauf und Resistenz gegenüber konventioneller Chemotherapie mit einer schlechten Ansprechrate ...
Therapiestandards: aktuelle Entwicklungen
Die Therapiestandards beim Mantelzelllymphom (MCL) sind aktuell im Wandel: Vor Kurzem erfolgten Zulassungen von Inhibitoren der Bruton-Tyrosinkinase (BTKi) in Kombination mit ...
Thrombotisch-thrombozytopenische Purpura: neue Therapiekonzepte
Die thrombotisch-thrombozytopenische Purpura (TTP) ist eine seltene, potenziell lebensbedrohliche thrombotische Mikroangiopathie, charakterisiert durch Thrombozytopenie, ...