T-Prolymphozyten-Leukämie (T-PLL): Welche Entwicklungen gibt es?
Autor:
OA Priv.-Doz. Dr. Georg Hopfinger
Wiener Gesundheitsverbund – Klinik Favoriten
3. Med. Abteilung – Zentrum für Onkologie und Hämatologie
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Die seltene T-Prolymphozyten-Leukämie (T-PLL) zeichnet sich durch einen meist aggressiven Verlauf und Resistenz gegenüber konventioneller Chemotherapie mit einer schlechten Ansprechrate aufalkylierende Substanzen oder CHOP aus. Neue Wirkstoffe und Kombinationen konnten die Therapie zwar verbessern. Doch der einzige kurative Ansatz ist derzeit eine allogene Stammzelltransplantation.
Keypoints
-
Alemtuzumab, intravenös verabreicht, gilt derzeit als Standardtherapie der T-PLL.
-
Eine allogene Stammzelltransplantation sollte als kurativer Ansatz möglichst frühzeitig erwogen werden.
-
Neue Therapieansätze wie MDM2-Inhibitoren (z.B. Idasanutlin) oder CAR-T-Zell-Therapie werden eventuell in Zukunft die Therapie der T-PLL verbessern.
Diagnostik der T-PLL
Die T-Prolymphozyten-Leukämie (T-PLL) ist mit einer Inzidenz von 1–2 Neuerkrankungen/1 Million selten, das mediane Erkrankungsalter liegt bei 65 Jahren. Klinisch zeigt die T-PLL einen meist aggressiven und refraktären Verlauf, eine indolente Frühphase wird nur selten beobachtet. Neben einer rasch zunehmenden Lymphozytose und Splenomegalie werden Lymphadenopathie und gelegentlich Hautinfiltrate beobachtet. Auf molekularer Ebene finden sich typischerweise chromosomale Aberrationen, welche die Loci 14q32.1 (TCL1A) oder Xq28 (MTCP1) involvieren.1 Es finden sich ein T-post-thymischer Immunphänotyp mit Expression von cyTCL1+ (>90%), CD3+ (>80%), CD5+ (100%), CD7+ (>90%), CD4+ (60%), CD8+ (15%) CD4+CD8+(25%) und in >70% eine spezifische Überexpression des Onkogens TCL-1. In einer internationalen Kooperation wurden Diagnose- und Therapiekriterien erarbeitet,2 sie sind in Tabelle 1 dargestellt. Die Diagnose einer T-PLL gilt als gesichert, wenn alle drei Hauptkriterien erfüllt sind oder wenn die ersten zwei Hauptkriterien und ein Nebenkriterium erfüllt sind.
Therapie der T-PLL
Eine Therapieindikation besteht bei Erfüllung eines der folgenden Kriterien:2 B-Symptome, Hb<10g/dl und/oder Thrombozytopenie <100000/µl, symptomatische oder stark zunehmende Lymphome, nachgewiesene extranodale Manifestationen, rasch zunehmende Lymphozytose (z.B. >30000/µl mehr als >50% in zwei Monaten oder Verdopplung innerhalb von sechs Monaten).
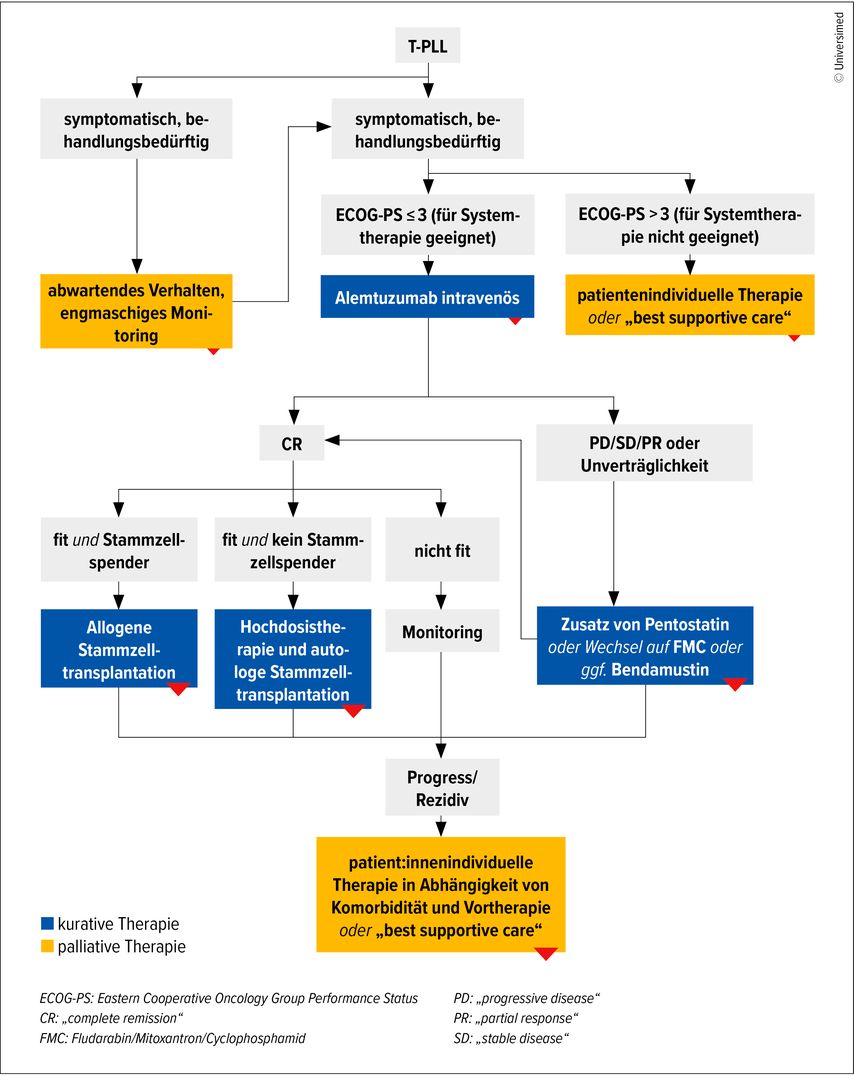
Das klinische Bild der T-PLL ist durch einen meist aggressiven Verlauf und Resistenz gegenüber konventioneller Chemotherapie mit einer geringen Ansprechrate von nur 30–45% auf alkylierende Substanzen oder CHOP charakterisiert. Der monoklonale Anti-CD52-Antikörper Alemtuzumab hat die Behandlungsergebnisse bei T-PLL deutlich verbessert. Bei rezidivierten Patient:innen führte Alemtuzumab als Monotherapie zu einer Gesamtansprechrate (ORR) von 76%, wobei 60% eine komplette Remission (CR) erreichten. Bei Einsatz als Erstlinientherapie wurde eine ORR von 91%, einschließlich 81% kompletter Remissionen, beobachtet.3
Mit dem Ziel einer weiteren Verbesserung initiierte die deutsche CLL-Studiengruppe eine prospektive Phase-II-Studie, in der eine Induktionstherapie mit Fludarabin, Cyclophosphamid und Mitoxantron (FMC) gefolgt von einer Alemtuzumab-Konsolidierungstherapie eingesetzt wurde.4 Nach FMC betrug die ORR 68%; nach intravenöser Alemtuzumab-Gabe stieg die ORR auf 92%, mit einem medianen progressionsfreien Überleben (PFS) und Gesamtüberleben (OS) von 11,9 bzw. 17,1 Monaten.5 Eine nachfolgende prospektive Studie mit FCM in Kombination mit subkutanem Alemtuzumab, gefolgt von einer subkutanen Alemtuzumab-Erhaltungstherapie, zeigte keine Verbesserung der Ansprechraten im Vergleich zur Kombination mit Chemotherapie. Daher wird – auch im Einklang mit anderen Studien – die intravenöse Applikation von Alemtuzumab bei T-PLL empfohlen (Abb.1).6
Wann immer möglich, sollte eine allogene Stammzelltransplantation (Allo-HCT), vorzugsweise in der ersten Remission, angestrebt werden. Eine Registerstudie der European Society for Blood and Marrow Transplantation (EBMT) mit 37 T-PLL-Patient:innen und einer CR-Rate von 62% vor Transplantation berichtet über ein vierjähriges rezidivfreies Überleben (RFS) von 30% und ein OS von 42%.7
Die Daten von 266 T-PLL-Patient:innen des Center for International Blood and Marrow Transplant Research (CIBMTR) zeigten eine Rate des krankheitsfreien Überlebens (DFS) über 4 Jahre von 25,7% und ein OS von 30%.8 Interessanterweise zeigte sich unter einer reduzierten Konditionierungsintensität (RIC) keine erhöhte Rezidivrate. Weiters waren mit einer Ganzkörperbestrahlung (TBI) keine signifikante Verlängerung des OS oder des DFS oder eine Verringerung der therapiebedingten Mortalität (TRM) assoziert.
Hoher Bedarf an neuen Therapieoptionen
Neue Therapieansätze erscheinen für die Behandlung der T-PLL dringend erforderlich. Ermutigende Pilotdaten aus „Drug-screening“-Studien konnten wertvolle Erkenntnisse liefern.
In einer Studie mit >2800 Einzelsubstanzen und Tumorproben von 30 T-PLL-Patient:innen zeigten sich bisher unbekannte „Drug“-Empfindlichkeiten von T-PLL-Zellen gegenüber mehreren Wirkstoffen wie dem Exportin-Inhibitor Selinexor, dem Makrolid Bafilomycin A1 (hemmt Autophagie und induziert Apoptose), Birinapant, einem SMAC-Mimetikum und Antagonisten von Inhibitoren apoptotischer Proteine (IAP), und Nutlin-3a (stabilisiert p53 und induziert Zelltod).9
In einer weiteren präklinischen Studie wurde die Inhibition von Histon-Deacetylasen (HDAC), BCL2, cyclinabhängigen Kinasen (CDK), „mouse double minute 2“ (MDM2) sowie klassische Zytostatika untersucht und darüber hinaus in zwei unabhängigen murinen Modellen (syngene Transplantate und patient:innenabgeleitete Xenografts) getestet.10 Interessanterweise zeigten sich auch synergistische Effekte in der Kombination von Cladribin mit dem HDAC-Hemmer Romidepsin, dem BCL2-Inhibitor Venetoclax und Idasanutlin, einem MDM2-Protein-Inhibitor, der durch eine Interaktion mit dem Tumorsuppressor p53 die Apoptose auslöst.
Ein weiterer Ansatz könnte die Verwendung von CAR-T-Zellen sein. Aktuell konnte eine sehr hohe Wirksamkeit von gentechnisch bearbeiteten (CRISPR-Cas9 edited) allogenen CAR-T-Zellen bei Patient:innen mit aggressiver T-ALL (akute lymphatische T-Zell-Leukämie) gezeigt werden. Die sogenannten allogenen Anti-CD7-WU-CART-007-Zellen sind gegen den T-Zell-Marker CD7 an Tumorzellen gerichtet. Bei den WU-CART-007 selbst wird CD7 deletiert, was eine Selbstzerstörung („fratricide“) der WU-CART-007-Zellen verhindert. Zudem wird die konstante Region der T-Zell-Rezeptor-α-Kette (TRAC) deletiert, wodurch das Risiko einer Graft-versus-Host-Erkrankung (GvHD) reduziert wird. In einer Phase-II-Studie (n=28) mit rezidivierter/refraktärer T-ALL/T-LBL erreichten 13 behandelte Patient:innen ein Gesamtansprechen von 90,9%.11
In einer weiteren Studie mit anderen T-Malignomen, die mit WU-CART-007 behandelt wurden, zeigten sich bei fünf Patient:innen, die bezüglich ihres Ansprechens ausgewertet werden konnten, zwei komplette Remissionen (CR; 1 PTCL, 1 T-PLL), zwei partielle Remissionen (PR; 1 T-PLL, 1 mit γδ-T-Zell-Lymphom) und eine stabile Erkrankung (γδ-T-Zell-Lymphom). Ein Patient starb an Mukormykose, ein Patient mit T-PLL befindet sich weiterhin in partieller Remission ohne Nachweis von Erkrankung und ein Patient mit T-PLL befindet sich zum Zeitpunkt der Präsentation (vier Monate nach der Behandlung) weiterhin in CR.12
Zusammenfassend ist festzustellen, dass die Ansprechraten nach Induktionstherapie mit intravenösem Alemtuzumab unbefriedigend bleiben, da die meisten Patient:innen selbst nach Erreichen einer kompletten Remission unter (Chemo-)Immuntherapie rezidivieren und nur ein Teil der Patient:innen mit einer allogen Stammzelltransplantation konsolidiert werden kann. Daher ist die rasche Umsetzung neuer therapeutischer Konzepte in multizentrischen Studiendesigns dringend erforderlich.
Literatur:
1 M Herling: T-Zell-Prolymphozytenleukämie; Oncopedia download 16.12.2025 2 Staber PB et al.: Consensus criteria for diagnosis, staging, and treatment response assessment of T-cell prolymphocytic leukemia. Blood 2019; 134(14): 1132-43 3 Dearden CE et al.: High remission rate in T-cell prolymphocytic leukemia with CAMPATH-1H. Blood 2001; 98(6): 1721-6 4 Dearden CE et al.: Alemtuzumab therapy in T-cell prolymphocytic leukemia: comparing efficacy in a series treated intravenously and a study piloting the subcutaneous route. Blood 2011; 118(22): 5799-802 5 Hopfinger G et al.: Sequential chemoimmunotherapy of fludarabine, mitoxantrone, and cyclophosphamide induction followed by alemtuzumab consolidation is effective in T-cell prolymphocytic leukemia. Cancer 2013; 119(12): 2258-67 6 Pflug N et al.: New lessons learned in T-PLL: results from a prospective phase-II trial with fludarabine-mitoxantrone-cyclophosphamide-alemtuzumab induction followed by alemtuzumab maintenance. Leuk Lymphoma 2019; 60(3): 649-57 7 Wiktor-Jedrzejczak W et al.: EBMT prospective observational study on allogeneic hematopoietic stem cell transplantation in T-prolymphocytic leukemia (T-PLL). Bone Marrow Transplant 2019; 54(9): 1391-8 8 Murthy HS et al.: Outcomes of allogeneic hematopoietic cell transplantation in T-cell prolymphocytic leukemia: a contemporary analysis from the Center for International Blood and Marrow Transplant Research. Transplant Cell Ther 2022; 28(4): 187.e1-187.e10 9 Pohly MF et al.: IAP dependency of T-cell prolymphocytic leukemia identified by high-throughput drug screening. Blood 2025; 145(20): 2336-52 10 von Jan J et al.: Optimizing drug combinations for T-PLL: restoring DNA damage and P53-mediated apoptotic responses. Blood 2024; 144(15): 1595-610 11 Ghobadi A et al.: Phase 1/2 trial of anti-CD7 allogeneic WU-CART-007 for patients with relapsed/refractory T-cell malignancies. Blood 2025; 146(10): 1163-73
Das könnte Sie auch interessieren:
Akute myeloische Leukämie (AML) – State of the Art 2025
Die aktuellen Therapiestandards der akuten myeloischen Leukämie ermöglichen eine spezifisch auf die Patient:innen abgestimmte Therapie, je nach Eignung für Chemotherapie und genetischem ...
Therapiestandards: aktuelle Entwicklungen
Die Therapiestandards beim Mantelzelllymphom (MCL) sind aktuell im Wandel: Vor Kurzem erfolgten Zulassungen von Inhibitoren der Bruton-Tyrosinkinase (BTKi) in Kombination mit ...
Thrombotisch-thrombozytopenische Purpura: neue Therapiekonzepte
Die thrombotisch-thrombozytopenische Purpura (TTP) ist eine seltene, potenziell lebensbedrohliche thrombotische Mikroangiopathie, charakterisiert durch Thrombozytopenie, ...