Schmerztherapie postpartal
Autorin:
Dr. med. Cora A. Vökt
SP Feto-Maternale Medizin; IBCLC
Frauenklinik Spital Grabs
E-Mail: cora.voekt@h-och.ch
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Paracetamol und nonsteroidale Antirheumatika (NSAR) werden seit Jahren routinemässig in der Schmerztherapie nach der Geburt zum Einsatz gebracht. Opioide kommen bei Bedarf ergänzend und in der Regel kurzfristig bei starken Schmerzen zur Anwendung.1 Es ist sinnvoll, auch solche seit Langem etablierten medikamentösen Therapieverfahren regelmässig zu hinterfragen, sich deren Wirkungs- und Nebenwirkungsspektren vor Augen zu führen sowie die Dosierung individuell anzupassen.
Basisanalgesie: Paracetamol 3–4 x 500mg/Tag ± Ibuprofen 3 x 400–600mg/Tag
Paracetamol ist ein bewährtes und gut verträgliches Analgetikum und Antipyretikum ohne antiphlogistische Wirkung. NSAR wirken zusätzlich antiphlogistisch.Die Dosis-Wirkungs-Kurve von Paracetamol ist wie auch die der NSAR flach, d.h., eine Dosiserhöhung bei Paracetamol von 500mg auf 1000mg führt zu einer nur geringen Verbesserung der akuten analgetischen Wirksamkeit. Neun von zehn Patientinnen müssen mit der doppelten Dosis behandelt werden, um bei einer eine zusätzliche Schmerzreduktion zu erreichen.2 Deshalb ist für Paracetamol grundsätzlich als Dosierung 3–4 x 500mg zu empfehlen.
Gemäss Embryotox ist in der Gruppe der NSAR Ibuprofen die erste Wahl während der Stillzeit. Eine Dosierung von Ibuprofen bis 1800mg/Tag ist in Kombination mit Paracetamol sinnvoll.3,4
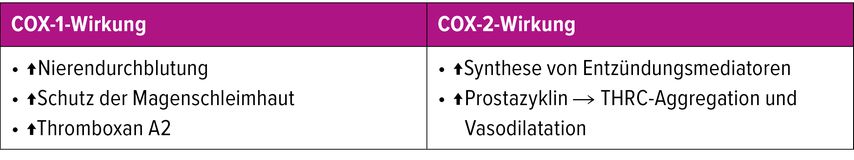
Das Nebenwirkungsspektrum ist bei beiden Substanzklassen ähnlich, da beide Cyclooxygenase-Inhibitoren sind: Paracetamol hemmt die Cyclooxygenase Typ 2 (COX-2) (Tab.1), in hoher Dosis auch COX-1. Ibuprofen ist ein nichtselektiver COX-1- und -2-Inhibitor (d.h. gleichermassen COX-1 und -2), welcher die Prostaglandin-Synthese sowie reversibel die Thrombozytenaggregation hemmt.
Dosen von 2–3g Paracetamol täglich oder die Kombination mit einem NSAR erhöhen das Risiko für gastrointestinale Ulkuskomplikationen. Paracetamol kann, analog den NSAR, den Blutdruck und das Risiko für eine arterielle Hypertonie erhöhen. Es verschlechtert auch geringfügig den Effekt einer antihypertensiven Therapie. Bei täglichem Gebrauch von Paracetamol ist das Risiko für einen Myokardinfarkt ähnlich wie bei den NSAR erhöht. Tagesdosen von mehr als 2g sind mit einem erhöhten Risiko für eine Herzinsuffizienz assoziiert, was insbesondere bei vorbestehender maternaler Herzerkrankung oder peripartaler Kardiomyopathie zu beachten ist.
Bei 4g/Tag treten häufig Leberenzymerhöhungen auf. Im Falle einer bereits vorgeschädigten Leber kann es innert weniger Tage zu einem akuten toxischen Leberversagen kommen. Deshalb ist bei maternalem HELLP-Syndrom besondere Vorsicht geboten. Bei Patienten mit einem sehr schlechten Ernährungszustand oder bei Alkoholabhängigkeit kann bereits eine normale Dosis zu einem Leberversagen führen.
Mögliche Auswirkungen auf das Stillkind
Es gibt für die Anwendung von Paracetamol keine nennenswerten Hinweise auf Unverträglichkeiten beim gestillten Kind. Maximal 2% der mütterlichen gewichtsadaptierten Dosis werden mit einer Stillmahlzeit aufgenommen. Der sogenannte Milch/Plasma(M/P)-Quotient liegt bei 0,8 bis 1,4. Ein M/P-Quotient von <1 gilt als niedrig, d.h., das Risiko für eine Anreicherung in der Muttermilch ist klein.
Auch bei Ibuprofen kommt es zu einem nur geringen Transfer in die Muttermilch (M/P von 0,2 bis 0,6). Die Anwendung gilt besonders in den ersten 24–72 Stunden post partum als sicher. Vorsicht ist allerdings bei Neugeborenen mit duktabhängigen Vitien geboten.
Opioidanalgetika sollten in der Stillzeit möglichst nur kurzfristig angewendet werden
Bei starken Schmerzen, welche durch die Basisanalgesie mit Paracetamol ± Ibuprofen unzureichend kupiert werden, ist die Einzelgabe bzw. kurzfristige Gabe eines Opioids unter guter Beobachtung des Stillkindes möglich.5,6
Die Dosis-Wirkungs-Kurve von Opioiden ist steiler als bei Paracetamol und den NSAR. Nur bei drei Personen unter Morphintherapie müsste man die Dosis erhöhen, um bei einer eine zusätzliche Schmerzreduktion zu erreichen.
Die Kombination eines Opioids mit Paracetamol erhöht die Wirksamkeit gegenüber Paracetamol oder Opioid alleine deutlich. Paracetamol reduziert damit bei gleicher Analgesiewirkung den Bedarf an Opioiden.
Morphin und Hydromorphon sind kurzfristig einsetzbar
Beide haben neben der analgetischen eine sedierende und antitussive Wirkung. Bei Anwendung im Rahmen einer Allgemeinanästhesie ist das Stillen erlaubt, sobald die Frau wieder bewusstseinsklar und selbst in der Lage ist, das Kind anzulegen. Der M/P-Quotient liegt bei 1,1–3,6, die Halbwertszeit bei 1,7 bis 4,5 Stunden. Morphin wird in der Leber durch Glucuronsäure inaktiviert und kann dann eliminiert werden. Da die Glucuronisierung in der kindlichen Leber in den ersten Lebenstagen noch eingeschränkt ist, verlängert sich die Eliminations-Halbwertszeit von Morphin beim Neugeborenen auf bis zu 14 Stunden (!). Eine Akkumulation ist möglich. Cave: atemdepressorische Wirkung besonders bei Kindern mit Apnoeneigung.
Codein kann als Antitussivum kurzzeitig (nicht länger als zwei bis drei Tage) eingenommen werden. Hauptmetabolit von Codein ist Morphin, welches durch Cytochrom P450 2D6 biotransformiert und dann in der Leber durch Glucuronsäure inaktiviert und eliminiert wird. Im Falle eines bestehenden genetischen Polymorphismus des CYP2D6-Allels kann es zu einer ultraschnellen Metabolisierung von Codein in Morphin kommen, was bereits bei geringen Dosen eine Opioidtoxizität bewirken kann. Beim gestillten Säugling sind hierdurch Apnoen, Cyanoseanfälle und Bradykardien auslösbar. Die Häufigkeit dieses genetischen Polymorphismus variiert in unterschiedlichen Populationen und liegt in Nordeuropa bei ca 4%, in Südeuropa bei 10% und in Teilen Afrikas bei ca. 16% der Bevölkerung. Auch Oxycodon wird durch Cytochrom P450 2D6 metabolisiert und ist mit analogen Risiken verbunden.
Gemäss Embryotox wird aufgrund diverser Fallberichte zu unerwünschten Wirkungen bei Stillkindern die Anwendung von Oxycodon in der Stillzeit nicht empfohlen. Einzeldosen sind vertretbar. Zu beachten ist auch die Interaktion mit anderen Medikamenten. Betablocker hemmen den Abbau von Oxycodon. Bei gleichzeitiger Anwendung von Cytochrom-Inhibitoren (z.B. Makrolidantibiotika) kommt es zu höheren Opioidkonzentrationen mit möglichen toxischen Nebenwirkungen wie Delir, Myoklonien und schwerer Atemdepression. In Kombination mit Enzyminduktoren (z.B. Carbamazepin, Phenytoin, Rifampicin) ist die analgetische Wirkung reduziert. Interaktionen bestehen ferner mit Ondansetron, Metoclopramid, Antidepressiva (z.B. Sertralin), Clonidin, Neuroleptika und Antiarrhythmika (z.B. Xylocain).
Opioide haben ein hohes Suchtpotenzial
Schwangerschaft und Elternschaft gelten als eine Lebensphase mit erhöhter Gefährdung für die Entwicklung einer Suchterkrankung. Eine verlängerte Opioidtherapie postpartal sollte deshalb möglichst vermieden werden.7
Durch aggressives Marketing von Herstellerfirmen hat die Verschreibung von Opioiden zwischen 1996 und 2012 in den USA stark zugenommen und zur sogenannten Opioidkrise mit seither rund einer Million Toten geführt. Der grösste Teil von ihnen war von Schmerzmitteln (u.a. Oxycodon) abhängig geworden, die zuvor verschrieben worden waren. Nachdem Oxycontin® (Oxycodon) vom Markt genommen worden war, stieg der illegale Konsum von Fentanyl in den USA, Kanada und Australien stark an. Fentanyl ist hochpotent, etwa zehnmal so stark wie Oxycodon, kostengünstig in der Herstellung und hat ein hohes Potenzial für illegalen Konsum und tödliche Überdosen.
Auch in der Schweiz ist der Opioidkonsum stark angestiegen. Gemäss einer ETH-Studie von Prof.Burden sind die hohen Verkaufszahlen von Oxycodon in der Schweiz vergleichbar mit denjenigen in Kanada in den frühen 2000er-Jahren.8,9
Individualisierte Therapie
Die postpartale Schmerztherapie sollte multimodal mit fixen Applikationsintervallen rund um die Uhr sowie individualisierter Medikation «on demand» erfolgen.
Nach vaginaler Geburt
Meist Dammverletzung und/oder Episiotomie als Schmerzursache: Lokale Applikation eines Coolpacks, Quarkwickel, Arnika-Gel auf Kompresse u.a. wirken supportiv. Im Rahmen der Wundversorgung bereits NSAR applizieren (z.B. Diclofenac 100mg supp. rektal).
Nachwehen
Wärme lokal, Magnesium per os, Chamomilla radix 2% Tabletten, Magnesium phosphoricum acidum, Potentilla anserina als Tee oder Bauchwickel werden als erleichternd empfunden.
Schmerzhafte Mamillen
Stilltechnik evaluieren, korrektes Andocken des Neugeborenen unterstützen, Stillposition variieren, Lokaltherapie mit Heilsalbe, Ausschluss einer Infektion
Nach Sectio in SPA/PDA
Neuraxiale Morphingabe essenziell (z.B. epidural 1,5–3mg/intrathekal 0,075–0,15mg), mit maternalem Monitoring auf Atemdepression (Überwachungsdauer abhängig von der applizierten Dosis und Substanz)
-
NSAR bei OP-Ende und in den ersten Tagen post partum fix, Paracetamol 4 x 500 mg
-
Bei Bedarf Einzeldosen von Morphin i.v./i.m/s.c./p.o. in den ersten 24–48 Stunden
-
In besonderen Fällen PCEA («patient controlled epidural analgesia»), z.B. mit Bupivacain 0,0625% plus Fentanyl 2mcg/ml
Nach Sectio in Intubationsnarkose
-
Basisanalgesie mit NSAR und Paracetamol
-
Wundinfiltration/Infusion mit Lokalanästhetikum
-
Bilateraler Nervenblock: Transversus abdominis plane (TAP) oder Quadratus lumborum (QL)10 – Block
-
PCA(«patient-controlled analgesia»)-Pumpe i.v. mit Morphin oder Hydromorphon für bis zu 24 Stunden, dann p.o. bei Bedarf (i.v. im Fall von Schmerzexazerbation)
Bei vorbestehendem (oder Z. n.) Opioidabusus
-
Neuraxiale Anästhesie sub partu/bei Sectio mit lang wirkendem Opioid (Morphin/Hydromorphon)
-
Paracetamol und NSAR fix
-
Ggfs. TAP- oder QL-Block, LA-Wundinfiltration, PCA oder PCEA
Bei Präeklampsie und HELLP-Syndrom
-
Neuraxiale Anästhesie, sofern möglich; PCEA oder PCA bei Bedarf postoperativ
-
Vermeiden von NSAR bei vorbestehender Nierenerkrankung oder erhöhtem Kreatinin
-
NSAR-Gabe ist bei hypertensiver Schwangerschaftserkrankung und Präeklampsie vertretbar und einer Opioidtherapie vorzuziehen.11,12
-
Vorsicht bei der Gabe von Paracetamol bei erhöhten Leberwerten
Zusammenfassung
Paracetamol und Ibuprofen gehören weiterhin zu den Schmerzmitteln der Wahl in der Stillzeit. Bei Bedarf ist – unter guter Beobachtung des Säuglings – kurzfristig die ergänzende Gabe eines Opioids möglich. Bei Entbindung per Sectio lässt sich durch die neuraxiale Morphingabe eine verlängerte postoperative Analgesie erreichen, sodass weniger systemische Opioidgaben nötig sind. Im Falle einer Sectio in Allgemeinanästhesie kann eine direkt postoperativ durchgeführte periphere Nervenblockade mittels Blocks des Transversus abdominis oder Quadratus lumborum die Notwendigkeit von postoperativen systemischen Opioidgaben wegen Schmerzexazerbation reduzieren. Eine Verordnung von Opioiden über den stationären Aufenthalt hinaus sollte vermieden werden.9
Literatur:
1 AWMF S1-Leitlinie zur geburtshilflichen Analgesie (001-038) 2020-AWMF Nr 001/0038S1 Leitlinie Geburtshilfliche Analgesie und Anästhesie 2 Liechti ME: Pharmakologie von Schmerzmitteln für die Praxis – Teil 1: Paracetamol, NSAR und Metamizol. Schweiz Med Forum 2014; 14(22-23):437-40 3 Shai Ram et al.: Paracetamol versus ibuprofen for early postpartum pain control: a randomized controlled trial. Arch Gynecol Obstet 2025; 312(1): 51-7 4 Ail-Kuraishy HM et al.: Paracetamol : the potential therapeutic pathways defining its clinical use. Inflammopharmacology 2025; 33(6): 2907-18 5 AWMF S3-Leitlinie Behandlung akuter perioperativer und posttraumatischer Schmerzen 9/2021 6 Macias DA et al.: Original Research : A comparison of acute pain management strategies after cesarean delivery. Am J Obstet Gyn 2022; 226(3): 407.e1-7 7 Matone M et al.: Postpartum persistent opioid use after opioid exposure for childbirth. Obstet Gynecol 2025; doi: 10.1097/AOG.0000000000006127 8 Hooijman MF et al.: Opioid sales and opioid-related poisonings in Switzerland: A descriptive population-based time-series analysis. Lancet Reg Health Eur 2022; 20: 100437 9 Rainer M et al.: Optimizing deprescribing of hospital-initiated opioids: a multi-level consensus study bridging evidence, expertise, and patient perspectives. Sci Rep 2025; 15(1): 35850 10 Oluwaseyi A et al.: Local anaesthetic wound infiltration for postcesarean section analgesia. A systematic review and meta-analysis. Eur J Anaesthesiol 2016; 33(10): 731-42 11 AWMF 015/018 S2k-Leitlinie Hypertensive Erkrankungen in der Schwangerschaft (HES): Diagnostik und Therapie 12 Gestational hypertension and preeclampsia. ACOG Practice Bulletin Number 222. 2020; 135: e237
Das könnte Sie auch interessieren:
Moderne Technik: das Wohl der Patientinnen im Mittelpunkt
Nach zweijähriger Pause präsentierte Prof. Volker Viereck das aktuelle Programm zum Thema Urogynäkologie in der Kartause Ittingen. Experten aus dem In- und Ausland beleuchteten ...
Relevantes für die gynäkologische Sprechstunde
Haarausfall (Effluvium) am Kapillitium wird von Betroffenen in aller Regel als belastend erlebt und führt vielfach zu einer Beeinträchtigung der Lebensqualität.1–4 Auch in der ...
Folsäure und Spina bifida
Auch in Zeiten der modernen Perinatalmedizin bleibt die Spina bifida eine folgenschwere Fehlbildung. Die konsequente perikonzeptionelle Folsäureprophylaxe ist eine Präventionsmassnahme ...